Клинические рекомендации по первичному гиперпаратиреозу, краткая версия
Первичный гиперпаратиреоз (ПГПТ) — эндокринное заболевание, характеризующееся избыточной секрецией паратиреоидного гормона (ПТГ) при верхненормальном или повышенном уровне кальция крови вследствие первичной патологии околощитовидных желез (ОЩЖ). ПГПТ проявляется полиорганными нарушениями различной степени выраженности и, как следствие, может приводить к существенному снижению качества жизни, инвалидизации пациентов, повышенному риску преждевременной смерти. Гиперкальциемия и катаболическое действие ПТГ на клетки различных органов рассматриваются как основные патогенетические механизмы развития осложнений при ПГПТ. За последние десятилетия отмечено резкое увеличение заболеваемости ПГПТ, в основном за счет выявления мягких форм заболевания, что прежде всего обусловлено совершенствованием методов диагностики и внедрением скрининга кальциемии в странах Северной Америки, Западной Европы и Азии. Увеличение выявляемости ПГПТ, многообразие клинических проявлений и форм этого заболевания привело к тому, что эти пациенты стали попадать в поле зрения различных специалистов — терапевтов, ревматологов, урологов, нефрологов, кардиологов и других врачей. В статье изложены основные тезисы клинических рекомендаций по ведению пациентов с ПГПТ, утвержденных Минздравом России в 2020 г. Изложены алгоритмы лабораторной и инструментальной диагностики, дифференциально-диагностических проб, рассмотрены вопросы хирургической и консервативной тактики ведения, динамического наблюдения за пациентами с данной нозологией. Отдельно выделены рекомендации для особых групп пациентов — наследственные формы ПГПТ, злокачественное поражение ОЩЖ, течение ПГПТ при беременности.
Ключевые слова
Для цитирования:
Мокрышева Н.Г., Еремкина А.К., Мирная С.С., Крупинова Ю.А., Воронкова И.А., Ким И.В., Бельцевич Д.Г., Кузнецов Н.С., Пигарова Е.А., Рожинская Л.Я., Дегтярев М.В., Егшатян Л.В., Румянцев П.О., Андреева Е.Н., Анциферов М.Б., Маркина Н.В., Крюкова И.В., Каронова Т.Л., Лукьянов С.В., Слепцов И.В., Чагай Н.Б., Мельниченко Г.А., Дедов И.И. Клинические рекомендации по первичному гиперпаратиреозу, краткая версия. Проблемы Эндокринологии. 2021;67(4):94-124. https://doi.org/10.14341/probl12801
For citation:
Mokrysheva N.G., Eremkina A.K., Mirnaya S.S., Krupinova J.A., Voronkova I.A., Kim I.V., Beltsevich D.G., Kuznetzov N.S., Pigarova E.A., Rozhinskaya L.Y., Degtyarev M.V., Egshatyan L.V., Rumiantsev P.A., Andreeva E.N., Аntsiferov M.B., Markina N.V., Kryukova I.V., Karonova T.L., Lukyanov S.V., Sleptcov I.V., Chagai N.B., Melnichenko G.A., Dedov I.I. The clinical practice guidelines for primary hyperparathyroidism, short version. Problems of Endocrinology. 2021;67(4):94-124. (In Russ.) https://doi.org/10.14341/probl12801
ВВЕДЕНИЕ
Первичный гиперпаратиреоз (ПГПТ) — эндокринное заболевание, характеризующееся избыточной секрецией ПТГ при верхне-нормальном или повышенном уровне кальция крови вследствие первичной патологии околощитовидных желез (ОЩЖ). ПГПТ проявляется полиорганными нарушениями различной степени выраженности и, как следствие, может приводить к существенному снижению качества жизни, инвалидизации пациентов, повышенному риску преждевременной смерти [1]. ПГПТ в 85–90% случаев обусловлен солитарной аденомой ОЩЖ, в 5–10% случаев — множественными аденомами или гиперплазией нескольких/всех ОЩЖ; в 1% — раком ОЩЖ. В 90–95% случаев ПГПТ является спорадическим, около 5–10% составляют наследственные формы, которые проявляются изолированной патологией ОЩЖ или протекают в сочетании с другими компонентами генетически детерминированных синдромов [2].
Патогенез опухолей ОЩЖ изучен недостаточно, в литературе обсуждается влияние некоторых протоонкогенов и генов супрессоров опухолевой активности на развитие новообразований. В качестве предположительных механизмов запуска гиперплазии с последующей трансформацией в аденому ОЩЖ рассматриваются хронический дефицит витамина D и усиление его инактивации в печени [3]. В ряде случаев спорадического ПГПТ определяются мутации в генах MEN1, CDC73, CASR, реже CDKIs, EZH2, POT1 [4].
ПГПТ, сопровождающийся множественными гиперплазиями или аденомами ОЩЖ, часто связан с наследственными синдромами. Синдром множественных эндокринных неоплазий 1 типа (МЭН-1) ассоциирован с мутациями в гене-супрессоре опухолевого роста MEN1; синдром МЭН-2 — с мутациями протоонкогена RET; синдром МЭН-4 развивается вследствие мутации ингибитора циклинзависимой киназы CDNK1B [5]. Синдром гиперпаратиреоза с опухолью нижней челюсти (HPT-JT) ассоциирован с мутациями в гене CDC73, кодирующем белок парафибромин [6]. Семейный изолированный гиперпаратиреоз (FIHP) характеризуется развитием опухолей одной или нескольких ОЩЖ и отсутствием других новообразований эндокринных и неэндокринных органов, иногда может представлять собой неполный вариант других синдромов (МЭН-1, HPT-JT). FIHP может быть обусловлен мутациями в генах MEN1, CASR и CDC73, но чаще генетическая причина остается неизвестной [7]. Семейная гипокальциурическая гиперкальциемия (FHH) — генетически гетерогенное заболевание, обусловленное мутациями в генах CASR, Gα11, AP2S1, требует проведения дифференциальной диагностики с ПГПТ [5].
За последние десятилетия произошли существенные изменения в представлениях об эпидемиологии заболевания. Отмечено резкое увеличение выявляемости ПГПТ, в том числе за счет бессимптомных форм, не сопровождающихся высокой гиперкальциемией. Указанные изменения обусловлены прежде всего появлением автоматических биохимических анализаторов и активным внедрением повсеместного определения уровня кальция в странах Северной Америки, Западной Европы и Китае. В общей популяции распространенность ПГПТ составляет в среднем 0,86–1% [8]. ПГПТ может встречаться во всех возрастных группах, включая детей и подростков. Однако совокупность фактических данных свидетельствует о том, что частота возникновения ПГПТ увеличивается с возрастом, и средний возраст на момент постановки диагноза составляет 54–59 лет [9]. Большинство пациентов при спорадическом ПГПТ — женщины в постменопаузе с развитием заболевания в течение первого десятилетия после наступления менопаузы. Соотношение мужчин и женщин в среднем 1:3 [9].
У большей части пациентов в Российской Федерации гиперкальциемия диагностируется отсроченно, поскольку определение содержания кальция не входит в общетерапевтический биохимический анализ крови. Это создает предпосылки для позднего выявления гиперпаратиреоза. В Российской Федерации широкомасштабных эпидемиологических исследований не проводилось. По результатам анализа 1914 пациентов с ПГПТ (Российский регистр пациентов с первичным гиперпаратиреозом) на декабрь 2017 г. наблюдается возрастание распространенности заболевания по г. Москве. В 2017 г. она составила 13 случаев на 100 000 взрослого населения (2016 г. — 5,6 случая, на 2010 г. — 4 случая на 100 000 взрослого населения). По Московской области распространенность ПГПТ на декабрь 2017 г. составила 3,4 случая на 100 000 взрослого населения (по сравнению с 2014 г. — 0,25 случаев). Несмотря на повышение распространенности, полученные данные не соответствуют частоте гиперкальциемии, обнаруженной по данным пилотного скрининга уровня кальция среди взрослого населения. В основном преобладали манифестные формы ПГПТ — в 67% случаев, бессимптомное течение заболевания определялось в 33%, в то время как в странах Европы, Северной Америки уже к 2004 г. частота манифестных форм не превышала 20%.
КЛАССИФИКАЦИЯ ПЕРВИЧНОГО ГИПЕРПАРАТИРЕОЗА
Симптомный (манифестный) ПГПТ характеризуется наличием «классических» проявлений заболевания, к которым относят костные (остеопороз, низкотравматичные переломы и фиброзно-кистозный остеит) и висцеральные нарушения (нефролитиаз, язвенная болезнь верхних отделов слизистой желудочно-кишечного тракта (ЖКТ)). В настоящее время к пациентам с бессимптомным ПГПТ (ранее классифицировали как мягкую форму) относят лиц, не имеющих специфических проявлений заболевания, при этом диагностика заболевания, как правило, происходит на этапе рутинного скрининга кальция. Ряд исследований свидетельствует о возможности длительного доброкачественного течения бессимптомного ПГПТ у большинства пациентов. Однако у некоторых пациентов с течением времени отмечается прогрессирование заболевания с развитием специфической симптоматики [9].
Наиболее часто диагностируется гиперкальциемический вариант ПГПТ, характеризующийся повышением уровня кальция сыворотки крови в сочетании с повышенным (редко высоко-нормальным) уровнем интактного ПТГ (иПТГ). Однако ПГПТ не всегда сопровождается повышением уровня кальция крови выше верхней границы референсного диапазона. Нормокальциемия может быть транзиторной при гиперкальциемическом варианте и стойкой при нормокальциемическом варианте заболевания. Нормокальциемический вариант ПГПТ (нПГПТ) характеризуется неизменно верхненормальным уровнем общего и ионизированного кальция (Са ++ ) в сыворотке крови в сочетании со стойким повышением уровня иПТГ, в отсутствие очевидных причин вторичного гиперпаратиреоза (ВГПТ) (дефицит витамина D, патология печени и почек, синдром мальабсорбции, гиперкальциурии и др.) [9][10]. Классификация ПГПТ представлена на рис. 1.

Рисунок 1. Классификация ПГПТ
КРИТЕРИИ ПОСТАНОВКИ ДИАГНОЗА ПЕРВИЧНОГО ГИПЕРПАРАТИРЕОЗА
- Диагноз гиперкальциемической формы ПГПТ рекомендуется устанавливать у пациентов при наличии гиперкальциемии в сочетании со стойким повышением уровня иПТГ или высоконормальным уровнем иПТГ (на верхней границе референсного интервала, но не выходящий за его пределы), исключив семейную доброкачественную гипокальциурическую гиперкальциемию с целью решения о проведении дополнительного обследования и выбора оптимальной тактики лечения [11–13].
- Диагноз нПГПТ рекомендуется устанавливать у пациентов при наличии следующих критериев [14–27]:
-стойкое сохранение показателей альбумин-скорректированного и Са ++ в референсном диапазоне за весь период наблюдения при повышенном уровне иПТГ (минимум двукратное определение в интервале 3–6 мес);
-исключение возможных вторичных причин гиперпаратиреоза (прежде всего дефицита/недостаточности витамина D (25(ОН)D ≤30 нг/мл) и ХБП (СКФ) ≤60 мл/мин));
УУР С (УДД — 4)
ЖАЛОБЫ И АНАМНЕЗ
- Определение уровня кальция сыворотки крови рекомендуется пациентам, имеющим одно или несколько из следующих клинических состояний и/или признаков, с целью принятия решения о дальнейшем обследовании на предмет исключения или верификации ПГПТ:
-клинические симптомы гиперкальциемии, включая инсипидарный синдром (полиурия/никтурия/полидипсия, не обусловленные сахарным или несахарным диабетом); тошноту, рвоту, снижение аппетита, дегидратацию [28][29];
УУР С (УДД — 4)
-остеопороз или предшествующие низкотравматичные переломы в анамнезе (особенно переломы шейки бедра, переломы дистального отдела костей предплечья), клинические проявления фиброзно-кистозного остеита, включая деформации скелета, боли в ребрах [30–34];
УУР В (УДД — 3)
-нефролитиаз (особенно рецидивирующий), нефрокальциноз [34–40];
УУР В (УДД — 2)
-рецидивирующая язвенная болезнь желудка или двенадцатиперстной кишки, калькулезный панкреатит [41–43].
УУР C (УДД — 4)
Комментарии: клинические проявления ПГПТ в большинстве случаев обусловлены гиперкальциемией. Легкая гиперкальциемия (общий кальций 3–3,5 ммоль/л (12–14 мг/дл)) при хроническом течении может протекать с минимальной симптоматикой. Быстро прогрессирующая гиперкальциемия может сопровождаться ухудшением состояния в виде появления таких симптомов, как полиурия, полидипсия, дегидратация, снижение аппетита, тошнота, мышечная слабость. У пациентов с тяжелой гиперкальциемией (общий кальций сыворотки крови >3,5 ммоль/л (14 мг/дл)) отмечается высокий риск гиперкальциемического криза [44][45]. При сборе анамнеза необходимо учитывать прием препаратов, влияющих на фосфорно-кальциевый обмен таб. 1.
Нефролитиаз — одно из основных осложнений ПГПТ. В 10% случаев симптомный нефролитиаз при ПГПТ характеризуется рецидивирующим течением с частыми приступами почечной колики [40][46]. Распространенность ПГПТ среди больных с мочекаменной болезнью может значимо превышать общепопуляционные значения и достигать 3,2–5% [35–39]. Чаще стали диагностироваться «молчащие» формы заболевания (бессимптомный нефролитиаз/нефрокальциноз), выявляемые при проведении визуализирующих методов исследования (ультразвуковое исследование (УЗИ), компьютерная томография (КТ) почек) [47].
В настоящее время фиброзно-кистозный остеит как наиболее тяжелое костное проявление ПГПТ диагностируется значимо реже, тем не менее пациенты могут сообщать о множественных перенесенных низкотравматичных переломах, деформациях скелета и изменении походки. При бессимптомном течении ПГПТ патологические изменения скелета верифицируются, как правило, при снижении минеральной плотности кости (МПК) по результатам рентгенденситометрии [2][48].
Необходим тщательный сбор анамнеза касательно других симптомов, ассоциированных с ПГПТ, включая язвенную болезнь желудка и двенадцатиперстной кишки, гастроэзофагеальную рефлюксную болезнь, острый панкреатит, чаще ассоциированные с умеренной и тяжелой гиперкальциемией [49].
Проявления со стороны мышечной системы, включающие проксимальную мышечную слабость и атрофию, в настоящее время редки, но многие пациенты с ПГПТ предъявляют субъективные жалобы на повышенную утомляемость и генерализованную слабость [50–52]. Ранее к классическим психическим проявлениям ПГПТ относили тяжелое нарушение когнитивных функций и сознания, острый психоз, но они, как правило являются следствием тяжелой гиперкальциемии. В настоящее время все чаще сообщается об умеренных психических расстройствах, таких, как усталость, депрессия, эмоциональная лабильность, нарушения сна, ухудшение памяти и неспособность сконцентрироваться.
Необходим тщательный сбор персонального и семейного анамнеза при подозрении на синдромальные формы эндокринопатий.
ФИЗИКАЛЬНОЕ ОБСЛЕДОВАНИЕ
- Пациентам с подозрением на ПГПТ рекомендуется оценка общего физического состояния, роста (снижение роста на 2 см и более за 1–3 года или на 4 см и более за всю жизнь), нарушений походки, состояния мышц и скелета (деформации, переломы), наличия костных разрастаний в области лицевой части черепа, крупных суставов, трубчатых костей с целью выявления характерных проявлений заболевания со стороны костной системы [8][53].
УУР С (УДД — 5)
ЛАБОРАТОРНЫЕ ДИАГНОСТИЧЕСКИЕ ИССЛЕДОВАНИЯ
Диагноз ПГПТ основывается только на данных лабораторного обследования.
- Пациентам с впервые выявленной гиперкальциемией рекомендуется повторное определение уровня общего кальция, альбумина (с расчетом альбумин-скорректированного кальция) и/или Са ++ с целью исключения ложноположительных результатов лабораторных анализов [12][54][55].
УУР С (УДД — 4)
Комментарии: при подозрении на ПГПТ первоначально рекомендуется определение уровня альбумин-скорректированного кальция крови, при этом гиперкальциемия должна быть подтверждена более чем в одном измерении, прежде чем пациенту будет назначено расширенное обследование. Корректировка кальция на уровень альбумина крови необходима с целью исключения ложно завышенных или ложно заниженных показателей кальциемии при изменении концентрации плазменных белков [55]. Коррекция общего кальция рекомендуется при уровне альбумина менее 40 г/л и более 45 г/л. Ложных результатов можно также избежать путем прямого определения Са ++ [12]. Этот показатель менее вариабельный, однако для его определения необходимо специальное оборудование — анализатор с использованием ион-селективных электродов, доступность которого в клинических лабораториях может быть лимитирована.
Формулы для расчета альбумин-скорректированного кальция:
общий кальций плазмы (ммоль/л) = измеренный уровень общего кальция плазмы (ммоль/л) + 0,02 × (40 — измеренный уровень альбумина плазмы (г/л))
общий кальций плазмы (мг/дл) = измеренный уровень общего кальция плазмы (мг/дл) + 0,8 × (4 — измеренный уровень альбумина плазмы (г/дл))
коэффициент пересчета: [кальций] мг/дл × 0,25 = [кальций] ммоль/л
- С целью верификации диагноза пациентам с подозрением на ПГПТ рекомендуется определение уровня общего кальция, альбумина (с расчетом альбумин-скорректированного кальция) и/или Са ++ , исследование уровня паратиреоидного гормона в крови (иПТГ) [12][13][55–60].
УУР В (УДД — 3)
Комментарии: для пациентов с ПГПТ уровень иПТГ, как правило, повышен или находится на верхней границе референсного диапазона [12][13]. В случае приема лекарственных средств, способных влиять на уровень кальция и/или иПТГ, проведение лабораторных тестов рекомендуется после отмены препаратов (табл. 1). Уровни иПТГ, находящиеся в нижнем диапазоне нормальных значений (
Таблица 1. Препараты, влияющие на показатели фосфорно-кальциевого обмена
Наименование препарата
Механизм действия
Увеличение реабсорбции Ca ++ в почках
Повышение порога чувствительности ОЩЖ с увеличением уровня кальция и иПТГ крови
Развитие гипокальциемии вследствие угнетения процессов костной резорбции
Развитие гипокальциемии вследствие угнетения процессов костной резорбции
Кальцимиметическое действие со снижением концентрации иПТГ и, как следствие, уменьшение содержания кальция в сыворотке крови
Рекомбинантный человеческий ПТГ, подобно эндогенному гормону увеличивает кишечную абсорбцию и канальцевую реабсорбцию кальция, потенциально может определяться в рамках гормонального анализа
Витамин D и его производные
Риск передозировки при уровне 25(ОН)D более 100 нг/мл
Назначение активных альфакальцидола** или кальцитриола** в дозе 0,5 мкг в сутки и более может способствовать развитию гиперкальциемии
У 1/3 пациентов выявляется гипофосфатемия за счет реципрокного отношения между кальцием и фосфором. Также для ПГПТ характерны повышенные или верхненормальные уровни общей щелочной фосфатазы и более специфичных маркеров костного метаболизма [10].
- С целью оценки фильтрационной функции почек и определения показаний к хирургическому лечению, а также для исключения вторичных причин повышения уровня иПТГ пациентам с подозрением на ПГПТ показано определение уровня креатинина с расчетом СКФ [58][61–63].
УУР С (УДД — 4)
Креатинин сыворотки считается важным диагностическим инструментом в когорте пациентов с ПГПТ, так как почки являются одним из основных органов регуляции обмена кальция и фосфора в организме. Клиренсовые радиоизотопные методики — золотой стандарт в определении СКФ, однако стоимость и технические сложности резко лимитируют их широкое применение. В клинической практике для расчета СКФ могут быть использованы простые способы расчета клиренса креатинина, позволяющие обойтись без суточного сбора мочи [64].
- Пациентам с ПГПТ рекомендуется определение уровня 25(ОН) витамина D c целью диагностики его недостаточности/дефицита [65–68].
УУР В (УДД — 3)
Комментарии: низкий уровень 25(ОН)D при ПГПТ ассоциирован с более высоким уровнем иПТГ и, как следствие уровнем кальция сыворотки крови, более низкой МПК в кортикальной зоне костей и более высокими показателями маркеров костного обмена, более частым развитием фиброзного остеита и большим весом аденомы ОЩЖ [65–67]. Оценка статуса витамина D проводится путем определения 25(ОН) витамина D в крови, что является наиболее доступным и надежным методом лабораторной диагностики [54].
- С целью верификации диагноза пациентам с ПГПТ и удовлетворительной фильтрационной функцией почек (СКФ>60 мл/мин/1,73 м 2 ) рекомендуется исследование уровней кальция и креатинина в моче (суточный анализ) с расчетом почечного клиренса кальция к клиренсу креатинина[11].
УУР В (УДД — 2)
Комментарии: измерение кальция в суточной моче по отношению к экскреции креатинина необходимо с целью дифференциальной диагностики ПГПТ и семейной гипокальциурической гиперкальциемии (FHH). FHH — это редкое наследственное заболевание с аутосомно-доминантным типом наследования, вызванное дефектом кальций-чувствительных рецепторов (CaSR) в почках и ОЩЖ. Диагноз FHH может быть заподозрен при сочетании гиперкальциемии, нормального или несколько повышенного уровня иПТГ и относительной гипокальциурии. Для дифференциальной диагностики используется расчет отношения почечного клиренса кальция к клиренсу креатинина (UCCR), который обычно при FHH составляет менее 0,01.
Формула для расчета почечного клиренса кальция к клиренсу креатинина [11]
CaCl/CrCl = [Cau x Crs]/[Cru x Cas]
CaCl — клиренс кальция, CrCl — клиренс креатинина, Cau — концентрация кальция в моче (ммоль/л), Crs — концентрация креатинина в сыворотке крови (мкмоль/л), Cru — концентрация креатинина в моче (мкмоль/л), Cas — концентрация кальция в сыворотке крови (ммоль/л)
Дополнительной ценностью данного анализа является определение суточной кальциурии, как показателя риска возникновения или прогрессирования нефролитиаза. При выявлении суточной экскреции кальция выше 10 ммоль/сутки показано проведение хирургического лечения ПГПТ. Необходимо отметить, что исследование кальция в моче не информативно при снижении функции почек (СКФ
- С целью дифференциальной диагностики между первичным нормокальциемическим и вторичным гиперпаратиреозом пациентам с сочетанием повышенного уровня иПТГ и нормокальциемией рекомендовано проведение функциональных проб [53][69–72].
УУР С (УДД — 4)
Комментарии: сочетание повышенного показателя иПТГ в крови с нормальным уровнем сывороточного кальция остается актуальной клинической проблемой. В целях дифференциальной диагностики между нормокальциемическим вариантом ПГПТ и ВГПТ, возникшим в результате недостаточности витамина D или при других состояниях [73, 74]. необходимо проведение функциональных проб (табл. 2) [15][16]. У пациентов с ПГПТ прием препаратов витамина D и его производных и/или гидрохлоротиазида** провоцирует развитие гиперкальциемии при сохранении повышенного уровня иПТГ, а у пациентов с ВГПТ–снижение/нормализацию уровня иПТГ при нормальном уровне кальция в крови [73][75]. При наличии гиперкальциурии целесообразно проведение пробы с тиазидами.
Таблица 2. Функциональные пробы для дифференциальной диагностики между первичной нормокальциемической и вторичной формами гиперпаратиреоза
Наименование препарата
Доза препарата
Интерпретация результатов
Сроки проведения
Пациентам с установленным дефицитом 25(ОН) витамина D c целью достижения целевого уровня витамина D более 30 нг/мл (75 нмоль/л)
Подтверждение ПГПТ: отсутствие снижения уровня иПТГ и в некоторых случаях появление гиперкальциемии.
Исключение ПГПТ: нормализация уровня иПТГ при уровне кальция в крови в референсном диапазоне 1
До достижения целевого уровня 25 (ОН) витамина D
Пациентам при нарушении обмена кальция и фосфора вследствие нарушения эндогенного синтеза 1,25 дигидроксиколекальциферола (активного метаболита витамина D)
1 мкг в сутки в течение 5–7 дней, анализ крови на 5–7-й день на кальций общий, альбумин, иПТГ.
При отсутствии гиперкальциемии продолжение пробы до 1 месяца 1
Подтверждение ПГПТ: отсутствие снижения уровня иПТГ и часто развитие гиперкальциемии
Исключение ПГПТ: нормализация уровня иПТГ при уровне кальция в крови в референсном диапазоне*
От 5–7 дней до 1 месяца
По 25 мг 2 раза в сутки в течение 2 недель.
Анализ крови на ПТГ на 15-й день
Подтверждение ПГПТ: отсутствие нормализации иПТГ и возможно, повышение уровня кальция сыворотки крови (нормализация через несколько суток после отмены препарата).
Исключение ПГПТ: нормализация уровня иПТГ
1 Возможно более длительное проведение пробы: при выявлении на 5–7-й день тенденции к снижению иПТГ и нормокальциемии продолжить пробу, при ПГПТ часто развитие гиперкальциемии — под контролем врача.
ИНСТРУМЕНТАЛЬНЫЕ ДИАГНОСТИЧЕСКИЕ ИССЛЕДОВАНИЯ
Диагноз ПГПТ устанавливается исключительно на основании результатов лабораторного обследования, данные визуализирующих методов исследования не должны рассматриваться как способ дифференциальной диагностики различных форм гиперпаратиреоза. Применение визуализирующих методов исследования обязательно только для подготовки пациентов к хирургическому лечению верифицированного гиперпаратиреоза. Цель предоперационной топической диагностики образования ОЩЖ при ПГПТ — подготовка к селективной паратиреоидэктомии. Для планирования эффективного хирургического лечения требуется информация о точном месте расположения образования ОЩЖ.
- Пациентам с ПГПТ в качестве первого этапа топической диагностики ОЩЖ рекомендуется проведение ультразвукового исследования (УЗИ) ОЩЖ [78–84].
УУР А (УДД — 1)
Комментарии: чувствительность УЗИ в случае солитарного образования ОЩЖ, по различным данным, варьируется от 76 до 91% и во многом зависит от квалификации специалиста [78–81]. Специфичность метода может достигать 96% [82–84]. Установлена высокая положительная прогностическая значимость и диагностическая точность УЗИ ОЩЖ (93,2% и 88% cоответственно) [78]. Аденома ОЩЖ, как правило, представляет собой образование округлой или овальной формы, гипоэхогенной структуры, очерченное изоэхогенной линией и контрастирующее с вышележащей гиперэхогенной тканью щитовидной железы. В ряде случаев могут визуализироваться кальцинаты и определяться кистозная дегенерация. В последнее время активно стали использовать УЗИ с контрастированием. Метод обеспечивает количественную и качественную оценку васкуляризации микрососудистого русла желез, что позволяет идентифицировать опухоли ОЩЖ. УЗИ с контрастированием обладает особыми преимуществами при наличии сопутствующего зоба, шейной лимфаденопатии, а также при полигландулярном поражении ОЩЖ даже после предшествующих хирургических вмешательств в области шеи [85].
Преимущества метода: отсутствие лучевой нагрузки; относительно низкая стоимость и высокая доступность исследования; возможность выявления сопутствующей патологии ЩЖ. Недостатки метода: значимая вариабельность диагностической точности метода в зависимости от квалификации специалиста; ложноположительные результаты за счет узловых образований ЩЖ или лимфатических узлов; значимые ограничения в проведении исследования при атипичной локализации ОЩЖ (например, за грудиной, в позадипищеводном пространстве).
- Пациентам с ПГПТ с целью функционально-топической диагностики образований ОЩЖ рекомендуется проведение сцинтиграфии ОЩЖ с технеция [ 99mTс ] сестамиби [78][80][86][87].
УУР А (УДД — 1)
Комментарии: длительное время стандартной методикой оставалась двухмерная планарная сцинтиграфия. В настоящее время все чаще используется трехмерная однофотонная эмиссионная компьютерная томография (ОФЭКТ) и гибридная технология ОФЭКТ/КТ, сочетающая в себе функциональную чувствительность ОФЭКТ с высокой анатомической детализацией многослойной КТ. Чувствительность метода может варьировать в широком диапазоне, от 54 до 96% [88], в среднем составляя около 88% в случае солитарного образования ОЩЖ [80]. Множественное поражение ассоциировано со значимым снижением чувствительности: до 33% при наличии двух аденом ОЩЖ и до 44% в случае гиперплазии 4 ОЩЖ [80]. Отсутствие визуализации аденом ОЩЖ при проведении сцинтиграфии при ПГПТ ассоциировано с повышенным риском полигландулярного поражения. Объединенная чувствительность и положительная прогностическая значимость для сцинтиграфии с технеция [ 99mTс ] сестамиби с ОФЭКТ составляют 79% (49–91%) и 91% (84–96%) соответственно [78]. Для ОФЭКТ/КТ отмечена большая чувствительность метода (86%, ДИ 81–90) при сравнении с ОФЭКТ (74%, ДИ 66–82) и двухмерной планарной сцинтиграфией (70%, ДИ 61–80), кроме того, данный метод имеет преимущество перед другими методиками в топической диагностике эктопированных образований [87].
Преимущества метода: определение локализации как типично расположенных, так и эктопированных образований ОЩЖ, в том числе в средостении (основываясь на специфичности метаболизма паратиреоидной ткани). Недостатки метода: значимая вариабельность диагностической точности исследования в зависимости от центра (опыта специалистов, технической оснащенности — планарная гамма-камера, ОФЭКТ, ОФЭКТ-КТ), где проводится исследование; возможные ложноположительные и ложноотрицательные результаты при наличии сопутствующих заболеваний щитовидной железы (аутоиммунный тиреоидит, многоузловой зоб, диффузно-токсический зоб, рак щитовидной железы); снижение чувствительности метода при поражении нескольких ОЩЖ; лучевая нагрузка.
Комбинация ОФЭКТ-КТ с технеция [ 99mTс ] сестамиби и УЗИ ОЩЖ экспертного класса на дооперационном этапе диагностики ПГПТ повышают чувствительность до 95–98%. В случае множественного поражения ОЩЖ чувствительность данной комбинации остается невысокой и составляет 30–60% [89].
- Пациентам с ПГПТ в случае отсутствия четкой визуализации образования ОЩЖ по результатам методов первой линии (УЗИ и радионуклидные исследования) рекомендуется проведение дополнительных методов исследования: КТ шеи и средостения с контрастным усилением [90], позитронной эмиссионной томографии (ПЭТ) всего тела с туморотропным радиофармацевтическим диагностическим средством [91];
УУР А (УДД — 1)
- магнитной резонансной томографии (МРТ) шеи [92][93].
УУР А (УДД — 2)
Комментарии: в спорных случаях, при расхождении результатов УЗИ и сцинтиграфии с технеция [ 99mTс ] сестамиби, применяется КТ шеи с внутривенным болюсным контрастированием. Традиционная КТ с контрастным усилением позволяет достаточно точно оценить размеры и локализацию образований ОЩЖ как в случае их типичного расположения, так и при наличии измененных эктопированных ОЩЖ, в том числе в средостении. Диагностическая чувствительность мультиспиральной КТ (МСКТ) сильно вариабельна и может составлять 46–87% [94]. Недостатками метода являются лучевая нагрузка, потенциальная нефротоксичность контрастного вещества и, соответственно ограниченное применение у пациентов с хронической болезнью почек (ХБП). Кроме того, исследование со стандартным шагом 5 мм возможно только при наличии желез массой 5 г и более, ошибка в данном случае не превышает 5%. В остальных случаях необходим более мелкий шаг снимков, что еще больше увеличивает лучевую нагрузку [95].
4D КТ демонстрирует многообещающие результаты в визуализации ОЩЖ, однако в настоящее время исследование малодоступно. Чувствительность метода 4D КТ составляет в среднем 89%, а положительная прогностическая значимость достигает 93,5% [78]. Относительно высокая чувствительность метода сохраняется при множественном поражения ОЩЖ — 62,5–85,7% [96–98]. Основными недостатками 4D-КТ являются высокая стоимость, значительное увеличение радиационного облучения, резко ограниченная доступность.
Проведение МРТ возможно для установления локализации патологически измененных ОЩЖ, однако данный метод обладает рядом недостатков: высокая стоимость, меньшая чувствительность (по разным данным, 43–71%, трудности в интерпретации полученных данных, что связано с возникновением артефактов при дыхательных движениях. Возможным преимуществом является выявление эктопированных в средостение ОЩЖ, но по точности данный метод уступает МСКТ [92][93].
Применение ПЭТ рекомендуется в отдельных случаях у пациентов с персистенцией заболевания или с рецидивом ПГПТ при отсутствии визуализации ОЩЖ с помощью других методов [91]. Однако данная методика является дорогостоящей и малодоступной, что препятствует ее широкому клиническому применению [99].
- В случае необходимости дифференциальной диагностики образований ОЩЖ с другими патологическими образованиями в области шеи (узлами щитовидной железы, лимфатическими узлами, кистами) пациентам с ПГПТ может быть рекомендована тонкоигольная аспирационная биопсия (ТАБ) ОЩЖ с последующим анализом уровня иПТГ в аспирате [100–103].
УУР А (УДД — 2)
Комментарии: данный метод полезен в случае необходимости дифференциальной диагностики образований ОЩЖ и узловых образований ЩЖ при отсутствии четкого подтверждения интратиреоидного расположения аденомы ОЩЖ по данным визуализирующих методик. Определение уровня иПТГ проводится с помощью стандартных наборов. Как правило, уровень иПТГ более 500 пг/мл соответствует патологически измененной ОЩЖ [103]. Цитологическое исследование ОЩЖ не проводится ввиду сложности дифференциальной диагностики с фолликулярными опухолями щитовидной желез. Кроме того, цитологическое исследование не позволяет дифференцировать доброкачественное от злокачественного поражения ОЩЖ [100–102].
ИНЫЕ ДИАГНОСТИЧЕСКИЕ ИССЛЕДОВАНИЯ
- Для определения спектра и тяжести костных нарушений пациентам с ПГПТ рекомендуется обследование, включая количественную оценку минеральной плотности кости (МПК) 3 отделов с помощью рентгеновской денситометрии, рентгенологическую оценку целостности скелета при подозрении на переломы, включая рентгенографию грудного и поясничного отдела позвоночника в боковой проекции при потере роста на 4 см с молодости или потере роста на 2 см за последний год [48][104–108].
УУР С (УДД — 5)
Комментарии: рентгенологическая картина костных поражений вследствие ПГПТ включает в себя субпериостальную резорбцию, кистообразование, гипертрофию надкостницы, деминерализацию костей черепа. Редкий, но специфичный симптом — образование «бурых» опухолей, чаще формирующихся в различных отделах скелета (бедро, таз, ключицы, ребра, челюсти, череп) [32][109]. Рентгенологическое обследование поясничного и грудного отделов позвоночника в боковой проекции необходимо для исключения или верификации компрессионных переломов тел позвонков [105].
В случае бессимптомного ПГПТ патологические изменения скелета выявляются при снижении МПК по результатам двухэнергетической рентгеновской абсорбциометрии (dual-energy X-ray absorptiometry, DEXA). Всемирная организация здравоохранения (ВОЗ) определяет остеопению как снижение МПК в интервале от 1 до 2,5 стандартных отклонения ниже пикового значения костной массы (Т- критерий в диапазоне от -1,0 до -2,5 SD) и остеопороз как снижение МПК, равное или большее чем 2,5 стандартных отклонения (Т-критерий
- Для определения спектра и тяжести поражения почек пациентам с ПГПТ рекомендуется проведение комплексного обследования, включая определение уровня креатинина с расчетом скорости клубочковой фильтрации (СКФ), определение уровня кальция в суточной моче и проведение УЗИ (КТ) забрюшинного пространства/почек [47][64][110–113].
УУР С (УДД — 4)
Комментарии: наличие структурных изменений почек является абсолютным показанием к проведению паратиреоидэктомии, таким образом, всем пациентам с ПГПТ рекомендуется выполнение УЗИ и/или КТ почек. КТ считается наиболее информативным методом в диагностике кальцификации почечной паренхимы [110].
Всем пациентам с ПГПТ необходим расчет СКФ. Почечная недостаточность является одним из наиболее тяжелых и малообратимых осложнений и связана с более выраженными клиническими проявлениями, повышением риска смерти, увеличением распространенности артериальной гипертензии [19][61]. Снижение СКФ до ХБП 3-й стадии диагностируется у 17–20% с ПГПТ, при этом часть пациентов могут иметь бессимптомную форму заболевания [64].
Суточная гиперкальциурия характерна в большей мере для ПГПТ с нефролитиазом [111][112]. Радикально выполненная паратиреоидэктомия снижает риск прогрессирования или рецидивирования нефролитиаза, в связи с чем наличие выраженной гиперкальциурии более 10 ммоль/сут (более 400 мг/сут) стало рассматриваться в качестве показания к хирургическому лечению ПГПТ [113].
- Проведение эзофагогастродуоденоскопии для оценки состояния верхних отделов ЖКТ пациентам с ПГПТ рекомендуется при наличии соответствующей клинической симптоматики и/или в рамках подготовки к хирургическому лечению [114–117].
УУР С (УДД — 4).
ЛЕЧЕНИЕ ПЕРВИЧНОГО ГИПЕРПАРАТИРЕОЗА
Хирургическое лечение — единственный радикальный и эффективный метод лечения ПГПТ.
Хирургическое лечение ПГПТ рекомендуется:
- всем пациентам с симптомным (манифестным) ПГПТ [113][118–123];
(УУР B (УДД — 3);
- пациентам моложе 50 лет [124–128];
(УУР B (УДД — 3);
- пациентам при повышении уровня альбумин-скорректированного кальция в сыворотке крови на 0,25 ммоль/л (1 мг/дл) относительно верхней границы референсного диапазона, установленной в данной лаборатории, независимо от наличия/отсутствия клинической симптоматики [120][129–131].
(УУР C (УДД — 2);
- пациентам при наличии остеопороза: низкотравматичные переломы в анамнезе и/или рентгенологически верифицированные переломы тел позвонков; при снижении МПК в лучевой кости, проксимальном отделе бедра или поясничном отделе позвоночника менее -2,5 SD по Т-критерию у женщин в постменопаузе и мужчин старше 50 лет по результатам рентгеновской денситометрии [33][120][129][131–138];
(УУР А (УДД — 2)
- пациентам при наличии функциональной и/или структурной патологии почек: снижение СКФ менее 60 мл/мин/1,73 м 2 [61][63][123][139–143];
(УУР C (УДД — 4)
- пациентам при наличии суточной экскреция кальция более 10 ммоль (400 мг) в сутки; нефролитиаза/нефрокальциноза (включая бессимптомные формы) [74].
(УУР C (УДД — 5)
Комментарии: удаление патологически измененной/ых ОЩЖ является единственным радикальным методом лечения ПГПТ. Динамическое наблюдение и медикаментозная терапия менее экономически выгодны даже в случае бессимптомного ПГПТ [144–146]. Хирургическое лечение показано всем пациентам с классическими проявлениями заболевания [118–120]. Преимущества радикального лечения заключаются в нормализации уровня кальция и устранении ассоциированных с гиперкальциемией симптомов, значимом улучшении состояния костной ткани [120–122] и почек [113][123]. К дополнительным преимуществам можно отнести улучшения со стороны сердечно-сосудистой и нейропсихических систем, заболеваний желудочно-кишечного тракта, однако это требует подтверждения в крупных рандомизированных контролируемых исследованиях [147]. Хирургическое лечение может быть рекомендовано в случае бессимптомного ПГПТ и в отсутствие показаний к паратиреоидэктомии при желании самого пациента, необходима оценка соотношения риска/пользы от операции. Результаты рандомизированных исследований свидетельствуют об улучшении качества жизни пациентов с бессимптомным ПГПТ после хирургического лечения [52][133][148].
Паратиреоидэктомия рекомендуется всем лицам моложе 50 лет, включая детей. В случае отказа от оперативного лечения пациентам моложе 50 лет потребуется более длительный период наблюдения, что ассоциировано с увеличением риска развития специфических осложнений заболевания и финансовых затрат.
Показатели эффективности хирургического лечения достигают 95–98% с частотой послеоперационных осложнений 1–2% при условии выполнения операции опытными хирургами. Показатели смертности при хирургическом лечении ПГПТ низкие. К наиболее серьезным послеоперационным осложнениям относятся парез возвратного гортанного нерва, транзиторная или стойкая гипокальциемия, кровотечение, отсутствие ремиссии заболевания [147]. Отсутствие эффекта после выполнения хирургического вмешательства, как правило, наблюдается в случае синдрома множественных эндокринных неоплазий, атипичного расположения образования ОЩЖ, рака ОЩЖ, отсутствия опыта у хирурга.
- Пациентам с ПГПТ и абсолютными показаниями к хирургическому лечению рекомендуется консультация врача-хирурга с целью решения вопроса об операции [53].
УУР C (УДД — 5)
- В случае четкой визуализации солитарного образования ОЩЖ и отсутствия факторов риска множественного или злокачественного поражения ОЩЖ пациентам с ПГПТ рекомендуется выполнение селективной паратиреоидэктомии [149–153].
УУР В (УДД — 3)
Комментарии: не так давно наиболее распространенными хирургическими вмешательствами при ПГПТ были «ревизионные операции» — односторонняя и двусторонняя ревизии шеи. Выбор таких объемов хирургического лечения был обусловлен низкой эффективностью топической диагностики и отсутствием методов интраоперационного контроля. Цель таких операций — не только удалить пораженную ОЩЖ, но и предотвратить возможные рецидивы ПГПТ. Однако любые «ревизионные операции» предполагали большую травматичность и риск интраоперационных осложнений [168 –171]. Кроме того, «ревизионные операции» приводили к большей частоте послеоперационного гипопаратиреоза (до 50%). После появления более совершенных методов топической диагностики, позволивших значительно улучшить результаты локализации пораженных ОЩЖ, основной операцией при ПГПТ и солитарном поражении стала селективная паратиреоидэктомия. При этой операции хирург удаляет только пораженную ОЩЖ, опираясь на данные предоперационного обследования [147]. Остальные железы не осматриваются и не травмируются. Селективная паратиреоидэктомия характеризуется высокой эффективностью (95–98%) и низким риском послеоперационных осложнений (1–3%) [149–152].
- В случае множественного поражения ОЩЖ, отсутствия визуализации ОЩЖ методами топической диагностики и адекватного снижения интраоперационного иПТГ рекомендована билатеральная ревизия шеи [154][155].
УУР С (УДД — 4)
Комментарии: при отсутствии четких топических данных о расположении измененной ОЩЖ, наличии множественного поражения ОЩЖ или отсутствии адекватного снижения интраоперационного иПТГ, а также пациентам с литий-индуцированным гиперпаратиреозом рекомендована двусторонняя ревизия шеи с удалением пораженных ОЩЖ [156–158].
- Для оценки радикальности проведения хирургического лечения пациентам с ПГПТ рекомендуется интраоперационное определение иПТГ сыворотки крови до и через 15 минут после удаления образования [159–164].
УУР А (УДД — 2)
Комментарии: интраоперационное исследование уровня иПТГ до и через 15 минут после удаления образования позволяет оценить радикальность проведенного вмешательства. Снижение уровня иПТГ позволяет хирургу закончить операцию и не проводить ревизию других областей. И наоборот, сохранение исходно высокого уровня иПТГ свидетельствует о сохранении источника(-ов) гиперсекреции ПТГ и требует проведения ревизии с целью их поиска [159–163]. Общая точность метода составляет около 80% [164], как и в случае предоперационной топической диагностики, наилучшие результаты отмечаются при солитарном образовании ОЩЖ (87–99%). При множественном поражении точность интраоперационного определения иПТГ снижается до 58% [164][165].
- В раннем послеоперационном периоде (на следующие сутки после паратиреоидэктомии) пациентам с ПГПТ рекомендуется контроль уровня альбумин-скорректированного кальция с целью своевременной диагностики послеоперационной гипокальциемии [84][154][166–173].
УУР В (УДД — 3)
Комментарии: после паратиреоидэктомии частота послеоперационной гипокальциемии может варьировать в широком диапазоне, от 5 до 47%. Снижение уровня кальция ниже референсного диапазона может быть обусловлено длительной супрессией нормальных ОЩЖ активной паратиромой, послеоперационным отеком оставшихся ОЩЖ или синдромом «голодных костей». Как правило, снижение уровня кальция ниже референсного диапазона носит транзиторный характер и может корректироваться в амбулаторном порядке [84][154][166–169]. Частота хронического гипопаратиреоза после первичного хирургического лечения крайне низкая, по данным различных исследований, составляет 0–3,6% [154][168][174]. Более низкий уровень кальция крови и более выраженная симптоматика отмечаются у пациентов, перенесших билатеральную ревизию шеи, по сравнению с лицами после минимально инвазивной паратиреоидэктомии [170][171].
Синдром «голодных костей», приводящий к выраженной гипокальциемии, как правило, развивается в раннем послеоперационном периоде у пациентов с тяжелыми костными проявлениями ПГПТ. К основным факторам риска развития синдрома относят пожилой возраст пациентов, рентгенологически верифицированные поражения костной ткани. Другими прогностически неблагоприятными факторами считаются вес и размер аденомы ОЩЖ. Данных об эффективной профилактике данного состояния представлено недостаточно [175].
Лечение препаратами витамина D и кальция рекомендовано пациентам с наличием симптомов гипокальциемии и/или снижением уровня альбумин-скорректированного кальция менее 2,1 ммоль/л (Са ++ менее 1,0 ммоль/л) [176–178]. Для устранения гипокальциемии, которая может сохраняться в течение нескольких месяцев после успешной паратиреоидэктомии, необходимы адекватная коррекция дефицита магния и нормализация обмена костной ткани. Предполагается, что предоперационное лечение бисфосфонатами (M05BA) снижает риски послеоперационной гипокальциемии, но на данный момент нет проспективных исследований, посвященных этой проблеме [84][175].
КОНСЕРВАТИВНОЕ ЛЕЧЕНИЕ
В настоящее время эквивалента хирургическому лечению ПГПТ не существует, поскольку ни один из применяемых препаратов не позволяет достичь равного эффекта по отношению к нормализации лабораторных показателей и улучшению МПК по сравнению с паратиреоидэктомией. Консервативное лечение ПГПТ с использованием медикаментозных препаратов в первую очередь направлено на коррекцию гиперкальциемии и профилактику гиперкальциемических кризов, предупреждение низкотравматичных переломов.
- Пациентам с бессимптомным течением ПГПТ и отсутствием показаний к хирургическому лечению может быть рекомендована консервативная тактика ведения c регулярным контролем следующих параметров [15][68][118][131][133][136][141][179–181]:
-уровень альбумин-скорректированного кальция крови — 2–4 раза в год;
-уровень креатинина крови с расчетом СКФ (СКD-EPI) — 1 раз в 6 мес;
-исследование уровня иПТГ — 1 раз в 6 мес;
-исследование уровня кальция в моче (суточный анализ) — 1 раз в 6 мес;
-УЗИ почек 1 раз в год (при необходимости КТ забрюшинного пространства);
-рентгеноденситометрия поясничного отдела позвоночника, рентгеноденситометрия проксимального отдела бедренной кости, рентгеноденситометрия лучевой кости; рентгенография грудного и поясничного отдела позвоночника в боковой проекции при подозрении на переломы тел позвонков (снижение в росте, появление болей в спине).
УУР C (УДД — 5).
Комментарии: предложения по динамическому наблюдению пациентов с бессимптомным ПГПТ основываются на результатах исследований, посвященных оценке и сравнению естественного течения заболевания с хирургической тактикой [15][68][118][131][133][136][179][180]. В настоящее время максимальный период наблюдения пациентов с ПГПТ без хирургического лечения составляет 15 лет [180]. Появление одного или более показаний для хирургического лечения за весь период наблюдения зафиксировано у 37% пациентов [180]. Данные по естественной прогрессии нПГПТ остаются ограниченными. В то время как одни исследователи сообщали о высоких показателях прогрессии в виде развития гиперкальциемии, нефролитиаза, гиперкальциурии, переломов и снижения МПК в течение небольшого периода наблюдения (22–41%) [15][68], другими авторами были получены противоположные результаты, свидетельствующие о низком риске ПГПТ-ассоциированных осложнений в данной когорте больных [10][182].
Всем пациентам рекомендуется диета с умеренным потреблением кальция и увеличением потребления жидкости до 1,5–2,0 л в сутки [183]. Резкое ограничение кальция в рационе необходимо в случае выраженной гиперкальциемии более 3 ммоль/л [184][185].
Имеются данные об использовании тиазидов в когорте пациентов с ПГПТ с целью коррекции гиперкальциурии и профилактики нефролитиаза/нефрокальциноза, нарушения почечной функции. Уменьшение суточной экскреции кальция на фоне минимальных и среднетерапевтических доз гидрохлоротиазида** у пациентов с ПГПТ не приводило к повышению показателей кальциемии [186][187]. Однако имеются свои ограничения в данной терапии.
- Консервативное лечение пациентов с симптомным ПГПТ или наличием показаний к паратиреоидэктомии может быть рекомендовано в следующих случаях [188–192]:
-при отказе пациента от хирургического лечения;
-при наличии противопоказаний к хирургическому лечению (тяжелые сопутствующие заболевания).
УУР C (УДД — 5)
- При невозможности выполнения хирургического лечения с целью коррекции гиперкальциемии и снижения потери костной массы пациентам с ПГПТ рекомендуется антирезорбтивная терапия (#алендроновая кислота**, 10 мг ежедневно или 70 мг 1 раз в неделю, #деносумаб 60 мг 1 раз в 6 мес п/к) и/или терапия цинакальцетом** [193–197].
УУР В (УДД — 2)
Комментарии: антирезорбтивная терапия показана пациентам с ПГПТ при снижении МПК в лучевой кости, проксимальном отделе бедра или поясничном отделе позвоночника ≤-2,5 SD по Т-критерию у женщин в постменопаузе и мужчин старше 50 лет по результатам рентгенденситометрии и/или при наличии низкоэнергетических переломов при невозможности выполнения хирургического лечения [193].
Бисфосфонаты (M05BA) снижают активность остеокластов, усиливая их апоптоз, и замедляют резорбцию кости [198]. На основании сходства патогенетических механизмов развития постменопаузального остеопороза и костных нарушений при ПГПТ было проведено несколько сравнительных исследований эффективности и безопасности пероральных бисфосфонатов (M05BA) (алендроновая кислота**) у больных ПГПТ. Данные о долгосрочной эффективности бисфосфонатов (M05BA) в отношении риска переломов ограничены отдельными исследованиями [199–201].
По результатам рандомизированного плацебо-контролируемого двойного слепого исследования 3-й фазы DENOCINA использование деносумаба** в дозе 60 мг 1 раз в 6 мес эффективно в отношении улучшения МПК и снижения скорости метаболизма костной ткани у пациентов с ПГПТ независимо от сочетанной терапии цинакальцетом** [196]. Деносумаб** имеет преимущество по сравнению с бисфосфонатами (M05BA) в отношении прироста МПК в кортикальной кости [202].
Цинакальцет** снижает уровень сывороточного кальция и иПТГ за счет повышения чувствительности CaSR к концентрации внеклеточного кальция. Использование цинакальцета** приводит к стойкой нормализации показателей кальциемии у 70–80% пациентов с ПГПТ [203]. Эффект может сохраняться в течение 5 лет, однако уровень сывороточного кальция возвращается к исходным значениям сразу после прекращения терапии. Данный препарат не влияет напрямую на показатели МПК и маркеры костной резорбции [203]. Убедительных данных о воздействии препарата на симптомы гиперкальциемии, нефролитиаз или качество жизни в литературе не представлено.
- Пациентам с ПГПТ и уровнем сывороточного кальция рекомендуется восполнение сопутствующего дефицита (недостаточности) витамина D на дооперационном этапе c помощью приема колекальциферола** с целью устранения вторичного повышения иПТГ, улучшения состояния костной ткани, а также профилактики развития тяжелой послеоперационной гипокальциемии; пациентам с ПГПТ и уровнем кальция >3 ммоль/л (>12 мг/дл) не рекомендуется восполнение сопутствующего дефицита (недостаточности) витамина D до проведения успешной паратиреоидэктомии ввиду отсутствия данных о безопасности назначения препарата [204].
УУР A (УДД — 2)
- Пациентам с ПГПТ после паратиреоидэктомии в случае сопутствующего дефицита/недостаточности витамина D рекомендуется терапия колекальциферолом** c целью устранения вторичного повышения уровня иПТГ и улучшения состояния костной ткани [126][205].
УУР A (УДД — 2)
Комментарии: для устранения вторичного повышения иПТГ на фоне дефицита витамина D рекомендуется поддерживать показатели 25(ОН)D на уровне не менее 20 нг/мл (50 нмоль/л), оптимальным считается уровень >30 нг/мл (75 нмоль/л) [17][206][207]. После успешной паратиреоидэктомии у ряда пациентов сохраняется повышенный уровень иПТГ, что может быть обусловлено имеющимся дефицитом/недостаточностью витамина D [208–211]. Достижение оптимального уровня витамина D после радикальной операции способствует нормализации уровня иПТГ, адекватной реабсорбции кальция и улучшению показателей МПК [126][205].
- Пациентам с ПГПТ, перенесшим хирургическое лечение, контроль показателей альбумин-скорректированного и/или Са ++ , креатинина, исследование уровня иПТГ рекомендуется проводить через 1 мес после операции, при наличии сопутствующего дефицита 25(ОН)D рекомендуется увеличение активного периода наблюдения с оценкой лабораторных показателей до 2–3 мес с целью достижения целевого уровня витамина D [209][211][212].
УУР В (УДД — 3)
ГИПЕРКАЛЬЦИЕМИЧЕСКИЙ КРИЗ
- Пациентам с ПГПТ, осложненным развитием гиперкальциемического криза, рекомендовано проведение хирургического лечения в срочном порядке, после интенсивной предоперационной подготовки, направленной на коррекцию гиповолемии и снижение гиперкальциемии [213–220].
УУР С (УДД — 4)
Комментарии: резкое повышение уровня кальция в сыворотке крови может приводить к развитию гиперкальциемического криза и провоцируется тяжелыми интеркуррентными состояниями: развитием инфекционных заболеваний, переломов, длительной иммобилизацией, приемом антацидных средств [213][214]. Гиперкальциемический криз, как правило, отмечается при повышении уровня альбумин-скорректированного кальция более 3,5 ммоль/л (Са ++ более 1,8 ммоль/л)* и характеризуется симптомами полиорганной дисфункции, включая поражение ЖКТ (анорексия, тошнота, неукротимая рвота с развитием дегидратации, острая боль в животе, острый панкреатит), почек (олигурия, острая почечная недостаточность, почечная колика), сердечно-сосудистой системы (нарушение проводимости и сердечного ритма, укорочение интервала Q–T), нервной системы (миалгии, мышечная слабость, спутанность сознания, ступор, кома до 40% случаев) [213–219].
Своевременное лечение пациентов с гиперкальциемическим кризом имеет решающее значение, так как это состояние ассоциировано с высоким уровнем летального исхода [213][215]. Гиперкальциемический криз при ПГПТ является показанием для проведения операции в срочном порядке. Консервативная тактика в отношении пациентов с тяжелой гиперкальциемией должна рассматриваться в качестве «подготовки» к оперативному лечению и, по возможности, проводиться в условиях отделения реанимации и интенсивной терапии [213–219]. Для уменьшения риска общей анестезии используются консервативные методы, направленные на коррекцию гиповолемии, стимулирование почечной экскреции кальция и торможение ускоренной резорбции костной ткани (табл. 3). Оптимальные сроки для паратиреоидэктомии у пациентов с гиперкальциемическим кризом остаются дискутабельными. Основываясь на результатах топических методов диагностики, селективная паратиреоидэктомия может рассматриваться в качестве оптимальной тактики для большинства пациентов. Тем не менее тяжелая гиперкальциемия/гиперкальциемический криз в 4,5–12% случаев могут быть обусловлены наличием карциномы ОЩЖ.
Таблица 3. Консервативное лечение тяжелой гиперкальциемии
Препарат
Функция
Предостережения
Отмена кальций-повышающих лекарственных средств
Натрия хлорид** 300–500 мл/ч (2–6 л/сут, ежедневно 1–3 дня) до полного возмещения дефицита жидкости и восстановления диуреза
Увеличивает фильтрацию и выделение кальция.
Понижает кальциемию на 0,25–0,75 ммоль/л
Избегать гипергидратации у пациентов с сердечно-сосудистой патологией
#фуросемид** 20–40 мг внутривенно по необходимости (диурез не менее 200–300 мл/ч) [221]
Целесообразно назначение у пациентов с риском кардиогенного отека легких. В этом случае, при достижении эуволемии, активная регидратация (например, 3 л 0,9% физиологического раствора в течение 24 ч) должна быть сбалансирована внутривенным введением фуросемида для поддержания водного баланса.
Также ингибирует реабсорбцию кальция в дистальных канальцах
если внутрисосудистый объем жидкости не восстановлен
#деносумаб** 60 мг п/к [222]
Моноклональное человеческое антитело к лиганду рецептора активатора ядерного фактора каппа В (RANKL), антирезорбтивный эффект,
возможность применения при ХБП
Гипокальциемия, воспаление подкожножировой клетчатки в месте введения (редко)
Подавляют функцию и активность остеокластов и резорбцию кости
Нефротоксичны, противопоказаны при СКФ менее 35 мл/мин/1,73 м 2 , снижают уровень кальция, уровень фосфора. Максимальные эффекты — в течение 72 ч
Ибандроновая кислота 3 мг в/в болюсно в течение 15–30 с [223]
Цинакальцет** 30–360 мг/сут
внутрь ежедневно. Начальная доза 30 мг/сут с последующим титрованием каждые 2–4 нед до достижения оптимального уровня кальция (нормокальциемия или снижение альбумин-скорректированного кальция до уровня, не превышающего 0,25 ммоль/л (1 мг/дл) относительно верхней границы референсного диапазона)
Агонист кальций-чувствительного рецептора,
возможность применения при ХБП
Гипокальциемия, тошнота, рвота
МЕДИЦИНСКАЯ РЕАБИЛИТАЦИЯ
Специфических реабилитационных мероприятий в отношении пациентов с ПГПТ не разработано.
ПРОФИЛАКТИКА
- Проведение контрольной рентгенденситометрии для оценки прироста МПК рекомендуется пациентам с ПГПТ через год после хирургического лечения и далее 1 раз в год в течение 3 лет [118, 129, 133, 135, 180, 224–226].
УУР С (УДД — 4)
Комментарии: как правило, активное восстановление костного метаболизма, существенный прирост МПК (в среднем 5–10% за год) в зависимости от выраженности костных потерь и возраста пациента происходит в течение первых 2 лет после успешно проведенной паратиреоидэктомии. В этот период не требуется дополнительное лечение, за исключением поддержания адекватного уровня 25(ОН) витамина D, назначения альфакальцидола**/кальцитриола** и препаратов кальция [118][129][133][135][180][224][225].
- Пациентам с ПГПТ лечение осложнений заболевания (нефролитиаз/нефрокальциноз, язвенная болезнь желудка и двенадцатиперстной кишки, нарушения ритма и других нарушений) после успешно проведенной паратиреоидэктомии при необходимости рекомендуется проводить под наблюдением соответствующих специалистов [8][53].
УУР С (УДД — 5)
НАСЛЕДСТВЕННЫЕ ФОРМЫ ПЕРВИЧНОГО ГИПЕРПАРАТИРЕОЗА
До 10% случаев ПГПТ имеют наследственную природу (табл. 4). Наследственные формы ПГПТ характеризуются манифестацией в молодом возрасте и отсутствием гендерных отличий [5]. Молекулярно-генетическая диагностика позволяет своевременно поставить диагноз и начать скрининг компонентов синдрома и их лечение, что особенно важно для бессимптомных заболеваний.
Таблица 4. Наследственные синдромы, ассоциированные с развитием первичного гиперпаратиреоза
МЭН-1
МЭН-2А 1
МЭН-4
HPT-JT
FIHP 2
Гиперпаратиреоз — симптомы и лечение
Что такое гиперпаратиреоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Курашова О. Н., эндокринолога со стажем в 29 лет.
Над статьей доктора Курашова О. Н. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Эндокринолог Cтаж — 29 лет Кандидат наук
Клиника «Хелми»
Дата публикации 1 марта 2019 Обновлено 26 апреля 2021
Определение болезни. Причины заболевания
Гиперпаратиреоз — это эндокринное заболевание, развивающееся при чрезмерном количестве паратиреоидного гормона (паратгормона) в организме, который выделяется околощитовидными железами.
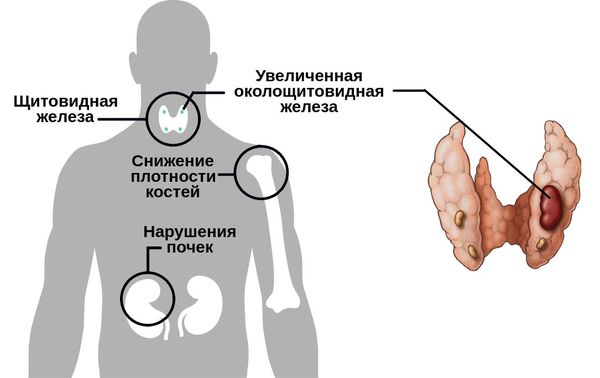
Существуют разные формы данного нарушения.
Первичный гиперпаратиреоз помимо нарушения околощитовидных желёз и избыточного выделения паратиреоидного гормона сопровождается верхне-нормальным или повышенным содержанием кальция в крови. Среди эндокринных заболеваний он встречается довольно часто: по распространённости эта форма гиперпаратиреоза находится на третьем месте после сахарного диабета и патологий щитовидной железы.
Ежегодная заболеваемость первичной формой составляет около 0,4–18,8% случаев на 10000 человек, а после 55 лет — до 2% случаев. [6] [12] У женщин эта патология возникает чаще, чем у мужчин — примерно 3:1. Преобладающее число случаев первичного гиперпаратиреоза у женщин приходится на первое десятилетия после менопаузы.
Первичный гиперпаратиреоз может быть как самостоятельным заболеванием, так и сочетаться с другими наследственными болезнями эндокринной системы. [1] [12] Он проявляется многосимптомным поражением различных органов и систем, что приводит к значительному снижению качества жизни с последующей инвалидизацией, а также к риску преждевременной смерти.
Причины возникновения связаны с развитием в одной или нескольких околощитовидных железах таких патологий, как:
- солитарная аденома — до 80-85% случаев;
- гиперплазия (диффузное увеличение желёз) — до 10-15 % случаев;
- рак — до 1-5% случаев;
- спорадические заболевания — до 90-95% случаев.
В 5% случаев на возникновение первичного гиперпаратиреоза влияет наследственность.
При вторичном гиперпаратиреозе кроме общих клинических признаков заболевания отличается снижением кальция и повышением фосфора в крови. Эта форма болезни обычно развивается как реакция компенсации и сочетает в себе усиленный синтез паратгормона и изменения в паращитовидных железах. Как правило, обнаруживается при синдроме недостаточного всасывания кальция в тонком кишечнике, дефиците витамина D и хронической почечной недостаточности.
Третичный гиперпаратиреоз развивается в случае аденомы околощитовидной железы и повышенном выделении паратгормона в условиях длительного вторичного гиперпаратиреоза.
Псевдогиперпаратиреоз развиваться п ри других злокачественных опухолях, которые способны продуцировать вещество, похожее на паратгормон.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы гиперпаратиреоза
Гиперпаратиреоз протекает длительно и бессимптомно и может быть выявлен случайно во время обследования по поводу другого заболевания.
У пациентов с гиперпарат иреозом одновременно возникают симптомы поражения различных органов и систем: язва желудка, остеопорозные проявления, мочекаменная и желчнокаменная болезни и другие. При пальпации шеи в зоне паращитовидных желёз можно нащупать достаточно большую «аденому».
Развивается быстрая утомляемость при физической повседневной нагрузке, мышечная слабость, ноющая головная боль, затруднение при ходьбе (особенно во время подъёма по лестнице или при преодолении больших расстояний), формируется как бы переваливающаяся походка.
У большинства людей с гиперпаратиреозом нарушено восприятие и память, они эмоционально неуравновешенны, тревожны, депрессивны.
При опросе пациенты с подозрением на нарушение функции околощитовидных желёз обычно жалуются на:
- длительно существующие боли в костях рук и ног, неровности и деформирующие изменения, возникающие при надавливании, частые судороги в ногах;
- эмоциональную неустойчивость, беспокойство и нарушение концентрации внимания, возникающее при нахождении в обществе;
- частое желание пить жидкость — вплоть до жажды с учащённым мочеиспусканием (не связанное с сахарным или несахарным диабетом);
- прерывистое нарушение сна и значительную утомляемость при выполнении любой работы;
- неуверенность и шаткость при ходьбе;
- повышенную потливость всего тела и конечностей;
- периодические сердцебиения днём и ночью;
- искривления и переломы (в основном трубчатых костей) при непредсказуемых обстоятельствах (даже при движениях лёжа в постели) — возникает в позднем периоде заболевания, сопровождается ноющими болями в позвоночнике.
Если патологический процесс в костях продолжает развиваться, это может стать причиной расшатывания и выпадения здоровых зубов, а также деформации костей скелета, в связи с которой пациенты становятся ниже ростом. Возникающие переломы очень медленно восстанавливаются, часто с деформациями р ук и ног и образованием непрочных суставов. На конечностях появляются кальцинаты — результат отложения солей.
У женщин с повышенной функцией щитовидной железы в менопаузе риск костных осложнений возрастает.
В большинстве случаев первые проявления гиперпаратиреоза сопровождаются:
- давно диагностированными нарушениями опорно-двигательного аппарата;
- хроническими заболеваниями почек (мочекаменная болезнь, отложение солей кальция в почках);
- нарушениями желудочно-кишечного тракта (панкреатит и кальцинат поджелудочной железы);
- выраженными, ранее нелеченными нейрокогнитивными и психическими расстройствами;
- артериальной гипертензией в сочетании с гипертрофией миокарда левого желудочка (утолщением стенок сердца), а также нарушением проводимости и ритма сердца — зависят от уровня паратгормона.
При развитии поражения сосудов в виде кальциноза и склероза нарушается питание тканей и органов, а повышенный уровень кальция в крови способствует развитию и ухудшению ишемической болезни сердца.
Гиперпаратиреоз с нехарактерными симптомами и постепенным началом часто сопровождается:
- тошнотой, периодическими желудочными болями, рвотой, метеоризмом, снижением аппетита, резким падением веса;
- возникновением пептических язв с кровотечениями;
- поражением поджелудочной железы и желчного пузыря;
- на поздних стадиях — нефрокальцинозом, признаками прогрессирующей почечной недостаточности с последующей уремией (крайне опасным отравлением организма).
Патогенез гиперпаратиреоза
Кальций является важным компонентом, который влияет на прочность костей и обменные процессы в организме. В норме уровень кальция, а также фосфора поддерживает паратгормон, выделяемый околощитовидными железами.
При аденоме или ином нарушении этих желёз взаимосвязь кальция и паратгормона нарушается: если раньше повышенное содержания кальция сдерживало уровень паратгормона, то теперь развивается дефект рецепторов, чувствительных к кальцию, которые расположены на поверхности главных клеток паращитовидных желёз.
В связи с этим в организме происходит ряд нарушений:
- активируются остеобласты (молодые клетки костей) и увеличивается количество остеокластов (клеток, уничтожающих старые костные ткани), что приводит к ускорению естественного разрушения (растворения) костей и костеобразования — если уровень паратгормона повышен довольно длительно, то процессы разрушения начинают преобладать;
- снижается почечный порог обратного всасывания фосфатов (проявляется гипофосфатемией и гиперфосфатурией);
- в кишечнике всасывается дополнительное количество кальция; [2][7][9]
- в случае гиперплазии (увеличения количества клеток паращитовидных желёз) происходит нерегулируемая гиперпродукция паратгормона. [17]
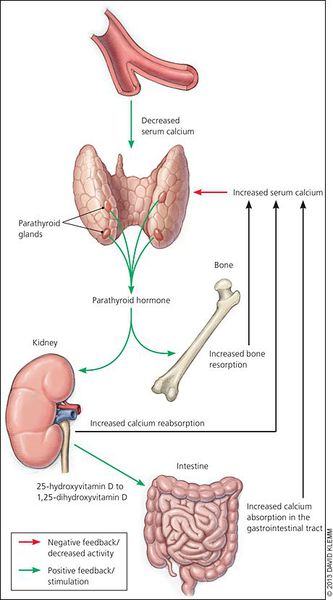
При избытке паратгормона усиливается выведение из костной ткани кальция и фосфора. Клинически это проявляется изменениями в костях: их искривлением и размягчением, возникновением переломов. При этом уровень кальция в костях снижается, а его уровень в крови заметно увеличивается, т. е. возникает гиперкальциемия. Она проявляется мышечной слабостью, избыточным выделением минералов с мочой при усиленном мочеиспускании и постоянной жаждой, что приводит к почечнокаменной болезни и нефрокальцинозу — накоплению и отложению солей кальция в главной ткани почек. Также избыток кальция в крови становится причиной нарушения тонуса сосудов и возникновения артериальной гипертензии. [1] [12]
У пациентов с первичным гиперпаратиреозом часто наблюдается острая нехватка витамина D, а после оперативного лечения заболевания повышается вероятность развития синдрома голодных костей — последствия гиперкальциемии. [15]
Классификация и стадии развития гиперпаратиреоза
Как уже говорилось, бывает первичный, вторичный и третичный гиперпаратиреоз. При этом первичную форму заболевания разделяют на три вида:
- субклинический — заболевание развивается без явных проявлений, можно заподозрить только по результатам биохимии крови;
- клинический — возникают выраженные симптомы болезни (нарушения опорно-двигательного аппарата, почек и ЖКТ);
- острый первичный — возникновение гиперкальциемического криза.
Согласно МКБ 10, выделяют четыре формы заболевания:
- первичный гиперпаратиреоз;
- вторичный гиперпаратиреоз;
- иные формы гиперпаратиреоза;
- неуточнённый гиперпаратиреоз.
Другая классификация гиперпаратиреоза, опубликованная в 2014 году, по степени выраженности симптомов разделяет заболевание на три формы:
- нормокальциемическую — определяется неизменными показателями общего и ионизированного кальция (с поправкой на альбумин), а также паратгормона за весь период наблюдения (двукратное определение этих показателей с интервалом в 3-6 месяцев);
- мягкую — можно установить при появлении жалоб (низкотравматичных переломов) и лабораторном подтверждении умеренно повышенного уровня кальция и паратгормона в крови;
- манифестную — возникает впервые, причём остро, сопровождается нарушениями костной ткани или внутренних органов, возникает риск развития гиперкальциемического криза.
В зависимости от того, какие именно органы или системы поражены, выделяют:
- костный гиперпаратиреоз — де формация конечностей, внезапные переломы, возникающие как бы сами по себе, остеопороз с возможными кистозными образованиями, болезнь Реклингхаузена;
- висцеральный гиперпаратиреоз — поражением внутренних органов:
- почечный — отличается тяжёлым течением, возникают частые приступы почечной колики, возможно развитие почечной недостаточности;
- желудочно-кишечный — холецистит, панкреатит, язвенная болезнь желудка и двенадцатиперстной кишки;
- смешанный гиперпаратиреоз — одновременное возникновение костных и висцеральных нарушений.
Осложнения гиперпаратиреоза
Длительное течение заболевания сказывается на формировании костей. Так, н а поздних стадиях вовремя не диагностированного гиперпаратиреоза наблюдаются:
- разрушение дистальных или концевых фаланг конечностей;
- сужение дистального отдела ключиц;
- очаги разрушения костей черепа;
- бурые опухоли длинных костей.
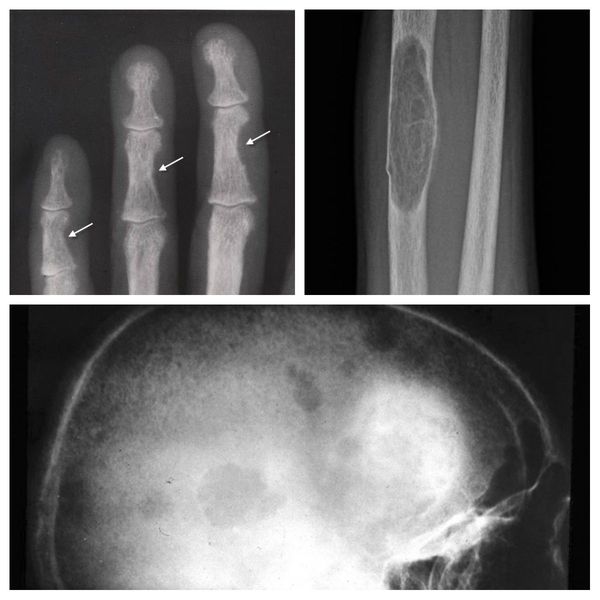
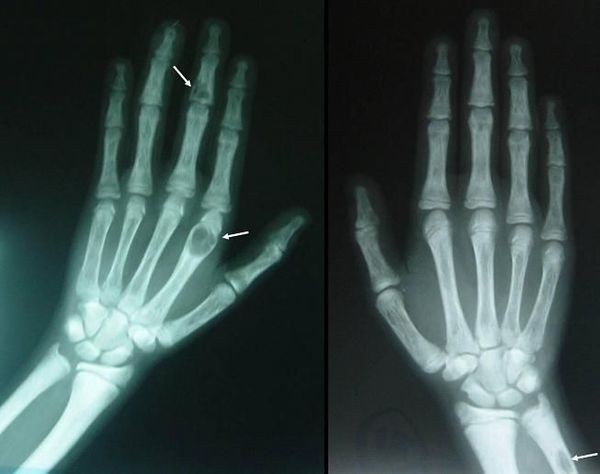
Самое тяжёлое осложнение гиперпаратиреоза — гиперкальциемический криз. Он возникает внезапно после резкого повышения уровня кальция в крови до 3,5-5 ммоль/л (в норме этот показатель составляет 2,15-2,50 ммоль/л). [17] Проявляется резким обострением всех симптомов гиперпаратиреоза.
Пусковые механизмы осложнения — острые инфекционные заболевания (чаще всего ОРВИ), внезапный перелом, длительный постельный режим, беременность, бесконтрольный приём препаратов, содержащих кальций и витамин D, а также тиазидных мочегонных средств.
Риск возникновения криза зависит от того, насколько повышен уровень кальция в крови. [17]
Источник https://www.probl-endojournals.ru/jour/article/view/12801
Источник https://probolezny.ru/giperparatireoz/