Острый инфаркт миокарда неуточненный (I21.9)
Инфаркт миокарда (ИМ) — это острое заболевание, вызванное развитием очага ишемического некроза мышцы сердца, возникшего вследствие закупорки коронарной артерии тромбом. В дальнейшем развивается острое несоответствие между потребностью миокарда в кислороде и доставкой его по коронарной артерии (абсолютная или относительная недостаточность коронарного кровотока).
Критерии острого инфаркта миокарда
Термин ИМ используется, когда присутствуют признаки некроза миокарда, согласующиеся в клинической картине с ишемией миокарда. При таких условиях диагнозу ИМ соответствует любой из нижеперечисленных критериев:
1. Выявление подъема и/или падения уровня сердечных биохимических маркеров (преимущественно тропонина), а также при наличии признаков ишемии миокарда одновременно с одним из следующих признаков:
— симптомы ишемии;
— визуализация признаков новой потери жизнеспособности миокарда или новой региональной аномалии движения стенки;
— изменения ЭКГ, указывающие на новую ишемию (новые ST-T изменения или новая блокада левой ножки пучка Гиса (БЛНПГ));
— развитие патологических зубцов Q на ЭКГ.
2. Внезапная сердечная смерть (ВСС), включающая остановку сердца. Часто она имеет симптомы, предполагающие ишемию миокарда, и сопровождается, вероятно, новым подъемом ST или вновь возникшей БЛНПГ, и/или со свидетельством наличия свежего тромба на коронарографии и/или аутопсии . Однако смерть наступает еще до того, как становится возможным получить образцы крови или в то время, когда сердечные биохимические маркеры еще не появились в крови.
3. Для аортокоронарного шунтирования (АКШ) у пациентов с нормальным уровнем тропонина подъем сердечных маркеров служит указателем на перипроцедурный некроз миокарда. Признаками ИМ вследствие АКШ являются:
— подъем уровней биохимических маркеров больше, чем в пять раз по отношению к норме;
— патологические зубцы Q либо БЛНПГ;
— ангиографически задокументированная окклюзия венечной артерии или шунта;
— визуализация признаков потери жизнеспособности миокарда.
4. При выполнении чрескожных вмешательств на коронарных артериях (ЧВКА) у больных с исходно нормальным уровнем тропонина, повышение концентрации специфических маркеров повреждения миокарда указывает на развитие некроза миокарда в ходе выполнения вмешательства. При увеличении концентрации биомаркеров более чем в 3 раза по сравнению с нормой принято диагностировать ИМ, связанный с выполнением ЧВКА. Выделяют также ИМ, обусловленный подтвержденным тромбозом стента .
5. Патоморфологические находки, которые свидетельствуют о наличии острого ИМ.
Критерии для постановки диагноза «первичный инфаркт миокарда»
Любой из приведенных ниже критериев соответствует диагнозу первичного ИМ:
— визуализация свидетельств о регионе потери жизнеспособности миокарда, то есть истончение стенки и утеря способности к сокращению, при отсутствии неишемических причин;
— развитие новых патологических зубцов Q с симптомами или без них;
— наличие вылеченного или лечащегося ИМ.
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
— 800 RUB / 5500 KZT / 27 BYN — 1 рабочее место в месяц
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
+7 938 489 4483 / +7 707 707 0716 / + 375 29 602 2356 / office@medelement.com
Мне интересно! Свяжитесь со мной
Классификация
Клиническая классификация различных типов инфаркта миокарда
| Тип 1 | Спонтанный инфаркт миокарда, связанный с ишемией вследствие первичного коронарного события, такого как эрозия и/или разрыв, трещина или расслоение бляшки. |
| Тип 2 | Инфаркт миокарда, вторичный по отношению к ишемии, возникшей либо из-за повышения потребности в кислороде, либо из-за снижения его доставки, например, из-за спазма коронарной артерии, коронарной эмболии, анемии, гипертонии или гипотонии. |
| Тип 3 | Внезапная сердечная смерть, включая остановку сердца, часто с симптомами, заставляющими предположить наличие ишемии миокарда, сопровождающимися новыми подъемами сегмента ST, или новой блокады левой ножки пучка Гиса, или признаками свежего тромба в коронарной артерии по данным ангиографии и/или аутопсии. Смерть наступает или до взятия проб крови, или до появления сердечных биомаркеров в крови. |
| Тип 4а | Инфаркт миокарда, связанный (ассоциируемый) с чрескожным коронарным вмешательством (ЧКВ). |
| Тип 4b | Инфаркт миокарда, связанный с тромбозом стента, что документировано ангиографией или аутопсией. |
| Тип 5 | Инфаркт миокарда, связанный с операцией аорто-коронарного шунтирования. |
В зависимости от размеров очагового поражения сердечной мышцы, выделяют два вида инфаркта миокарда:
— мелкоочаговый;
— крупноочаговый.
Около 20% клинических случаев приходится на долю мелкоочаговых инфарктов миокарда, однако часто мелкие очаги некроза в сердечной мышце трансформируются в крупноочаговый инфаркт миокарда (у 30% пациентов).
При мелкоочаговых инфарктах, в отличие от крупноочаговых, не возникают аневризма и разрыв сердца. Также течение мелкоочаговых инфарктов реже осложняется сердечной недостаточностью, тромбоэмболией , фибрилляцией желудочков .
В соответствии с глубиной некротического поражения сердечной мышцы различают следующие виды инфаркта миокарда:
— трансмуральный — с некрозом всей толщи мышечной стенки сердца (чаще крупноочаговый);
— интрамуральный – с некрозом в толще миокарда;
— субэндокардиальный – с некрозом миокарда в зоне прилегания к эндокарду;
— субэпикардиальный — с некрозом миокарда в зоне прилегания к эпикарду.
Согласно изменениям, фиксируемым на ЭКГ, выделяют:
— «Q-инфаркт» — с формированием патологического зубца Q, иногда желудочкового комплекса QS (чаще — крупноочаговый трансмуральный инфаркт миокарда);
— «не Q-инфаркт» – не сопровождается появлением зубца Q, проявляется отрицательными Т-зубцами (чаще — мелкоочаговый инфаркт миокарда).
По топографии и в зависимости от поражения определенных ветвей коронарных артерий, инфаркт миокарда бывает:
— правожелудочковый;
— левожелудочковый: передней, боковой и задней стенок, межжелудочковой перегородки.
По кратности возникновения инфаркт миокарда подразделяется на:
— рецидивирующий (развивается в срок до 8 недель после первичного);
— повторный (развивается спустя 8 недель после предыдущего).
По развитию осложнений инфаркт миокарда может быть:
— осложненный;
— неосложненный.
По наличию и локализации болевого синдрома различают следующие формы инфаркта миокарда:
— типичная – с локализацией боли за грудиной или в прекордиальной области ;
— атипичная — с атипичными болевыми проявлениями:
а) периферические: леволопаточная, леворучная, гортанно-глоточная, нижнечелюстная, верхнепозвоночная, гастралгическая (абдоминальная);
б) безболевые: коллаптоидная, астматическая, отечная, аритмическая, церебральная;
— малосимптомная (стертая);
— комбинированная.
В соответствии с периодом и динамикой развития инфаркта миокарда выделяют:
— стадию ишемии (острейший период);
— стадию некроза (острый период);
— стадию организации (подострый период);
— стадию рубцевания (постинфарктный период).
Этиология и патогенез
Непосредственной причиной развития инфаркта миокарда (ИМ) является остро наступающее несоответствие коронарного кровообращения запросам миокарда вследствие окклюзии Окклюзия — нарушение проходимости некоторых полых образований в организме (кровеносных и лимфатических сосудов, подпаутинных пространств и цистерн), обусловленное стойким закрытием их просвета на каком-либо участке.
коронарной артерии или резкого уменьшения притока крови по ней с последующей ишемией и некрозом.
Инфаркт миокарда с патологическими зубцами Q (тромботическая окклюзия коронарной артерии) развивается у 80% больных с инфарктом миокарда и приводит к трансмуральному некрозу миокарда и появлению зубца Q на ЭКГ.
Инфаркт миокарда без патологических зубцов Q наиболее часто возникает при спонтанном восстановлении перфузии Перфузия — 1) продолжительное нагнетание жидкости (например, крови) с лечебной или экспериментальной целью в кровеносные сосуды органа, части тела или всего организма; 2) естественное кровоснабжение некоторых органов, например почек; 3) кровообращение искусственное.
или хорошо развитых коллатералях Коллатераль — анатомическое образование, соединяющее структуры в обход основного пути.
. Размер инфаркта в этом случае меньше, функция левого желудочка страдает меньше, больничная летальность ниже. Однако частота повторных инфарктов миокарда выше, чем при инфаркте миокарда с патологическими зубцами Q, вследствие того, что такие инфаркты миокарда — «незавершенные» (то есть миокард, оставшийся жизнеспособным, снабжается пораженной коронарной артерией); к концу первого года летальность уравнивается. Поэтому при инфаркте миокарда без патологических зубцов Q следует придерживаться более активной лечебно-диагностической тактики.
В основе развития ИМ лежат три патофизиологических механизма:
1. Разрыв атеросклеротической бляшки, спровоцированный внезапным повышением активности симпатической нервной системы (резкое повышение артериального давления, частоты и силы сердечных сокращений, усиление венечного кровообращения).
2. Тромбоз на месте разорванной или даже интактной Интактный (Лат. intactus — нетронутый) — неповрежденный, не вовлеченный в какой-либо процесс.
бляшки в результате повышения тромбогенной способности крови (за счет усиления агрегации Агрегация — свойство тромбоцитов соединятся друг с другом.
тромбоцитов, активации коагулянтной системы и/или ингибирования фибринолиза Фибринолиз (Фибрин + греч. lysis — распад, разложение) — процесс растворения фибринового сгустка в результате ферментативных реакций; при тромбозе Фибринолиза приводит к канализации тромба.
).
3. Вазоконстрикция Вазоконстрикция — сужение просвета кровеносных сосудов, особенно артерий.
: локальная (участка коронарной артерии, где находится бляшка) или генерализованная (всей коронарной артерии).
Первый этап развития острого инфаркта миокарда (ОИМ), хотя и не всегда обязательный — разрыв атеросклеротической бляшки, который в дальнейшем может иметь различное течение:
1. Благоприятное течение — когда после разрыва бляшки происходит кровоизлияние в бляшку, так называемый «внутреннеинтимальный» тромб, что не вызывает развития инфаркта миокарда, но в дальнейшем может способствовать прогрессированию клинической картины ишемической болезни сердца (ИБС).
2. Неблагоприятное течение — с формированием тромба, который полностью или практически полностью перекрывает просвет венечной артерии.
Выделяют три стадии формирования тромба, обтурирующего Обтурация — закрытие просвета полого органа, в том числе кровеносного или лимфатического сосуда, обусловливающее нарушение его проходимости.
коронарную артерию:
1. Кровоизлияние в бляшку.
2. Формирование внутрисосудистого неокклюзирующего тромба.
3. Распространение тромба до полной закупорки сосуда.
Внутреннеинтимальный тромб состоит в основном из тромбоцитов. Формирование тромба является ключевым в развитии ОИМ.
Гораздо реже ОИМ возникает не как результат атеротромбоза. Ведущим патогенетическим механизмом в этом случае рассматривается вазоспазм Вазоспазм — сужение артерий или артериол до степени снижения перфузии тканей.
.
Инфаркт миокарда как результат коронароспазма Коронароспазм (Coronarospasmus; коронаро- -спазм) — временное сужение просвета венечных артерий сердца в результате тонического сокращения гладкомышечных элементов артериальной стенки; проявляется приступом стенокардии.
достаточно часто наблюдается у людей, принимающих наркотики, так называемый «кокаиновый» инфаркт миокарда.
Значительно реже инфаркт миокарда развивается в результате других причин.
Морфологические особенности
Инфаркт — заболевание всегда острое и стадийное. При инфаркте миокарда отмечают, что в первые сутки зона инфаркта внешне никак не отличается от здоровых участков миокарда. Зона инфаркта в это время носит мозаичный характер, то есть среди погибших клеток встречаются также частично или даже полностью работоспособные миоциты. На вторые сутки зона постепенно отграничивается от здоровой ткани и между ними формируется периинфарктная зона.
Часто в периинфарктной зоне различают зону очаговой дистрофии, граничащую с некротической зоной, и зону обратимой ишемии, примыкающую к участкам неповрежденного миокарда.
Все структурные и функциональные изменения в зоне очаговой дистрофии в большинстве случаев подлежат восстановлению (частично или даже полностью).
В зоне обратимой ишемии изменения бывают полностью обратимы. После отграничения зоны инфаркта наступает постепенное размягчение и растворение погибших миоцитов, элементов соединительной ткани, участков сосудов, нервных окончаний.
При крупноочаговом инфаркте миокарда примерно на 10-е сутки на периферии очага некроза уже образуется молодая грануляционная ткань, из которой в дальнейшем формируется соединительная ткань, выполняющая рубец. Заместительные процессы идут от периферии к центру, поэтому в центре очага какое-то время могут еще оставаться очаги размягчения, а это участок, который способен растягиваться, формируя аневризму сердца или даже разрываться при грубом несоблюдении двигательного режима или других нарушениях. В месте некроза плотная рубцовая ткань окончательно формируется не ранее чем через 3-4 месяца.
При мелкоочаговом инфаркте миокарда рубец иногда образуется в более ранние сроки. На скорость рубцевания влияют не только размеры очага некроза, но и состояние коронарного кровообращения в миокарде, в особенности в периинфарктных участках. Помимо этого, имеют значение следующие факторы:
— возраст больного;
— уровень АД;
— двигательный режим;
— состояние обменных процессов;
— обеспеченность пациента полноценными аминокислотами, витаминами;
— адекватность проводимого лечения;
— наличие сопутствующих заболеваний.
Все это определяет интенсивность восстановительных процессов в организме в целом и в миокарде в частности.
Даже относительно небольшая нагрузка в период формирования первичного рубца может привести к развитию аневризмы сердца (выпячиванию стенки желудочка, формированию своеобразного мешка), тогда как уже через месяц такая же нагрузка оказывается полезной и даже необходимой для укрепления сердечной мышцы и формирования более прочного рубца.
Эпидемиология
Признак распространенности: Очень распространено
Сегодня в развитых странах число пациентов с коронарной патологией постоянно растет, причем происходит сдвиг в сторону более молодого возраста, что делает проблему диагностики, лечения и профилактики ишемической болезни социально значимой.
Заболеваемость среди мужчин гораздо выше, чем среди женщин: в среднем 500 на 100 000 мужчин и 100 на 100 000 женщин, в возрасте старше 70 лет эта разница нивелируется.
Возрастной пик заболеваемости инфарктом миокарда — 50-70 лет.
У мужчин пик заболеваемости приходится на зимнее время, у женщин — на осень, снижение заболеваемости у мужчин и женщин происходит одновременно в летний период времени.
Самыми опасным временем суток у мужчин считаются предутренние часы (4-8 часов утра), когда частота развития ИМ достигает 23,9%; у женщин аналогичный показатель составляет 25,9% в утренние часы (8-12 часов). Такая частота развития ИМ в зависимости от сезонности и времени суток совпадает с аналогичными показателями «внезапной смерти».
Внезапная смерть обычно происходит в утренние часы при подъеме больного с постели, что вероятнее всего связано с повышением активности симпатической нервной системы при пробуждении. Это вызывает увеличение вязкости крови и агрегационную активность тромбоцитов с выбросом вазоактивных биологических веществ, за чем следует спазм сосудов и тромбообразование, с развитием ишемического инсульта или острого инфаркта миокарда (ОИМ).
Примерно одна треть всех случаев ОИМ (а у более молодых больных еще чаще) завершается летальным исходом на догоспитальном этапе, в большинстве случаев уже через 1 час после появления острых симптомов. Среди пациентов с ОИМ, доживших до поступления в больницу, в результате проведенной современной терапии отмечаются меньшая летальность и более продолжительная выживаемость.
Смерть больных ОИМ в первые 4 часа связана с появлением аритмий и развитием фибрилляции желудочков (аритмогенная смерть), а в более поздние сроки — с нарастанием острой сердечной недостаточности (кардиогенный шок).
Факторы и группы риска
Факторы риска развития инфаркта миокарда (ИМ) совпадают с таковыми при ишемической болезни сердца (ИБС).
Немодифицируемые факторы риска:
1. Наследственность. Считается отягощенной по ИБС, если у близких родственников (родители, братья, сестры, дедушки, бабушки) были случаи ИБС по мужской линии до 55 лет, по женской до 65 лет.
2. Возраст. В разных популяциях выявлена прямая зависимость между возрастом человека и частотой возникновения ИБС — чем старше человек, тем выше заболеваемость ИБС.
3. Пол. Мужчины гораздо чаще болеют ИБС. У женщин до 50-55 лет (возраст наступления стойкой менопаузы) ИБС диагностируется крайне редко. Исключение составляют женщины с ранней менопаузой и различными гормональными нарушениями при отягчающих обстоятельствах: артериальная гипертония , гиперлипидемия , сахарный диабет. После наступления менопаузы частота возникновения ИБС у женщин начинает неуклонно расти, и после 70-75 лет вероятность развития ИБС у мужчин и женщин одинакова.
Модифицируемые факторы риска:
1. Неправильное питание. Употребление пищи, богатой насыщенными жирами животного происхождения, с высоким содержанием поваренной соли и низким содержанием пищевой клетчатки.
2. Артериальная гипертония. Значение повышенного артериального давления, как одного из факторов риска, доказано многочисленными исследованиями во всем мире.
3. Гиперхолестеринемия . Повышенное содержание в крови общего холестерина, холестерина липопротеидов низкой плотности. Холестерин липопротеидов высокой плотности рассматривается как фактор антириска — чем выше его уровень, тем меньше риск возникновения ИБС.
4. Слабая физическая активность или отсутствие регулярных физических нагрузок. У людей, ведущих малоподвижный образ жизни, вероятность возникновения ИБС в 1,5-2,4 выше, чем у физически активных.
5. Ожирение. Особенно опасно ожирение по абдоминальному типу, когда жир откладывается в области живота.
6. Табакокурение. Прямая связь курения с развитием и прогрессированием атеросклероза хорошо известна и не нуждается в комментариях.
7. Сахарный диабет. Относительный риск смерти даже у лиц с нарушением толерантности к глюкозе выше на 30%, а у больных сахарным диабетом 2 типа — на 80%.
8. Злоупотребление алкоголем. Однако фактором антириска является употребление до 30 г чистого алкоголя в сутки для мужчин и 20 г — для женщин.
9. Во всем мире сейчас уделяется внимание изучению таких факторов риска, как хронический психоэмоциональный стресс, повышенная частота сердечных сокращений, нарушение системы свертываемости, гомоцистеинемия (повышение уровня в крови гомоцистеина ).
Ученые также установили зависимость риска развития инфаркта миокарда в зависимости от психо-эмоционального типа человека. Так, холерики имеют в 2 раза больше шансов получить первый инфаркт и в 5 раз больше — повторный, а смертность от инфаркта у них встречается в 6 раз чаще.
Провоцирующими моментами для развития острого инфаркта миокарда (ОИМ) являются интенсивное физическое или психоэмоциональное напряжение. На протяжении часа после значительного физического напряжения риск развития ОИМ возрастает в 6 раз, причем у лиц, ведущих малоподвижный образ жизни, — в 10,7 раза, а у лиц, занимающихся интенсивными физическими упражнениями, — в 2,4 раза. Подобным эффектом обладают и сильные переживания. В течение 2 часов после психоэмоционального перенапряжения риск развития ОИМ возрастает в 2,3 раза.
Частота развития ОИМ возрастает в утренние часы, в течение первого часа после пробуждения. Это касается и частоты развития внезапной смерти, инсульта, транзиторной ишемии миокарда, по данным Холтеровского наблюдения. Повышение риска связывают с увеличением в это время артериального давления и ЧСС , усилением агрегационных свойств тромбоцитов и снижением фибринолитической активности плазмы крови, повышением уровня катехоламинов , АКТГ , кортизола .
Похолодание и изменение атмосферного давления также способствуют повышению риска развития ОИМ. Так, при снижении температуры на 10°С, по сравнению со среднегодовой для данного времени года, риск развития первого ИМ возрастает на 13%, а повторного — на 38%. Изменения атмосферного давления, как в одну, так и в другую сторону, сопровождаются учащением развития ИМ на 11-12%, а повторного — на 30%.
Клиническая картина
Cимптомы, течение
Фазы острого инфаркта миокарда (ОИМ):
1. Продромальный период (длится до 30 суток, может отсутствовать).
2. Острейший период (продолжается до 2 часов от начала ангинозного статуса ).
3. Острый период (длится до 10 дней от начала инфаркта миокарда).
4. Подострый период (начинается с 10 дня и продолжается до 1-2 месяцев).
5. Период рубцевания (в среднем длится от 2-3 месяцев до полугода, иногда завершается лишь спустя 2-3 года).
В зависимости от стадии болезни ее проявления сильно варьируют.
Продромальный период
В этот период у пациентов развиваются признаки нестабильной стенокардии :
— учащаются боли в груди;
— боли появляются при меньших физических нагрузках, а то и вовсе в покое;
— боли хуже снимаются нитратами, требуется большая доза нитратов, чтобы боль прошла.
Острый коронарный синдром (ОКС) объединяет такие заболевания, как нестабильная стенокардия, острый инфаркт миокарда и внезапная сердечная смерть. В основе всех этих состояний, несмотря на разные их проявления, лежит один механизм. Как при инфаркте, так и при нестабильной стенокардии нарушается целостность одной из холестериновых бляшек в коронарной артерии. Организм реагирует на образовавшийся дефект, отправляя в очаг тромбоциты и активируя свертывающую систему крови. Как следствие, образуется тромб, перекрывающий ток крови. Кратковременное или неполное перекрытие просвета сосуда вызывает развитие симптомов нестабильной стенокардии . Если закупорка усугубляется, происходит инфаркт.
В связи с этим пациентов с нестабильной стенокардией необходимо экстренно госпитализировать.
Острейший период
В этот период наблюдается самая высокая летальность от инфаркта миокарда. В то же время, острейший период – самый благоприятный в плане терапии. Существуют препараты, которые разрушают образовавшийся тромб, тем самым восстанавливая нарушенный ток крови по сосуду. Однако эти лекарства эффективны лишь в течение первых 12 часов с момента развития инфаркта, и чем раньше они применены, тем лучше будет результат.
В острейший период появляется ангинозный статус — очень интенсивная боль, которая локализуется либо за грудиной, либо в левой половине грудной клетки. Пациенты описывают боль как кинжальную, сверлящую или давящую («сердце сжало в тисках»). Зачастую боль накатывает волнами, может отдавать в левое плечо, руку, межлопаточную область, нижнюю челюсть. Иногда она распространяется на правую половину грудной клетки и в верхнюю половину живота.
Боль в целом схожа с таковою во время приступа стенокардии, но интенсивность ее гораздо выше, она не проходит после приема 2-3 таблеток нитроглицерина и обычно длится от 30 минут и дольше.
Помимо боли нередко наблюдается холодный пот, выраженная общая слабость. Артериальное давление чаще снижается в результате уменьшения силы сокращений поврежденного сердца, реже — повышается, поскольку организм в ответ на стресс выбрасывает большое количество адреналина, оказывающего стимулирующее влияние на работу сердечно-сосудистой системы. Почти всегда при инфаркте миокарда пациенты испытывают выраженную тревогу, страх смерти.
Важно знать, что у 20% пациентов острейший период инфаркта протекает малосимптомно (так называемая «безболевая» форма инфаркта миокарда). Такие пациенты отмечают неясную тяжесть в груди («сердечную тоску»), выраженную утомляемость, недомогание, бессонницу, «беспричинную» тревогу.
Еще у части больных инфаркт миокарда может проявлять себя развитием нарушений ритма и проводимости. Такие пациенты ощущают перебои в работе сердца, возможно — резкое учащение, или, напротив, замедление пульса. Могут появляться головокружение, выраженная слабость, эпизоды потери сознания.
Иногда инфаркт миокарда может манифестировать внезапно возникшей одышкой или отеком легких.
Симптоматика клинических вариантов острейшей фазы инфаркта миокарда
| Болевой (status anginosus) |
Типичное клиническое течение, основным проявлением при котором служит ангинозная боль, не зависящая от позы и положения тела, от движений и дыхания, устойчивая к нитратам. Боль имеет давящий, душащий, жгущий или раздирающий характер с локализацией за грудиной, во всей передней грудной стенке с возможной иррадиацией в плечи, шею, руки, спину, эпигастальную область. Характерно сочетание с гипергидрозом, резкой общей слабостью, бледностью кожных покровов, возбуждением, двигательным беспокойством. |
| Абдоминальный (status gastralgicus) |
Проявляется сочетанием эпигастральных болей с диспептическими явлениями — тошнотой, не приносящей облегчения рвотой, икотой, отрыжкой, резким вздутием живота. Возможны иррадиация болей в спину, напряжение брюшной стенки и болезненность при пальпации в эпигастрии. |
| Атипичный болевой | Болевой синдром имеет атипичный характер по локализации (например, только в зонах иррадиации — горле и нижней челюсти, плечах, руках и т.д.) и/или по характеру. |
| Астматический (status astmaticus) |
Единственный признак — приступ одышки, являющийся проявлением острой застойной сердечной недостаточности (сердечная астма или отек легких). |
| Аритмический | Нарушения ритма служат единственным клиническим проявлением или преобладают в клинической картине. |
| Цереброваскулярный | В клинической картине преобладают признаки нарушения мозгового кровообращения (чаще — динамического): обморок, головокружение, тошнота, рвота. Возможна очаговая неврологическая симптоматика. |
| Малосимптомный (бессимптомный) | Наиболее сложный для распознавания вариант, нередко диагностируемый ретроспективно по данным ЭКГ. |
Острый период
В этом периоде острая боль стихает, поскольку процесс разрушения кардиомиоцитов завершен, а некротизированные ткани не чувствительны к боли. Большинство больных могут отмечать сохранение остаточных болей: глухих и постоянных, как правило, локализующихся за грудиной.
На вторые сутки ферменты из поврежденных клеток и разрушенные ткани попадают в кровь, вызывая температурную реакцию: может появляться лихорадка до 39°С, а также недомогание, слабость, потливость.
Действие стрессовых гормонов (адреналина, норадреналина, дофамина) утихает, в результате чего артериальное давление снижается, иногда очень значительно.
В этот период могут появляться тупые боли в груди, усиливающиеся при дыхании, что является признаком развития плевроперикардита. У части больных интенсивные давящие боли в сердце могут возобновиться — в таком случае диагностируется постинфарктная стенокардия либо рецидив инфаркта миокарда.
Поскольку рубец еще не сформирован, а часть мышечных клеток сердца разрушена, в этот период очень важно минимизировать физическую активность, стресс. При несоблюдении этих правил может развиться аневризма сердца или наступить смерть от разрыва сердца.
Подострый период
В этот период болевые ощущения, как правило, отсутствуют. Учитывая тот факт, что сократительная способность сердца снижена, поскольку участок миокарда «выключен» из работы, могут появиться симптомы сердечной недостаточности: одышка, отеки ног. В целом же состояние пациента улучшается: температура нормализуется, артериальное давление стабилизируется, риск развития аритмии уменьшается.
В сердце происходят процессы рубцевания: организм устраняет образовавшийся дефект, замещая разрушенные кардиомиоциты соединительной тканью.
Период рубцевания инфаркта миокарда
В этот период продолжается и завершается образование полноценного рубца из грубоволокнистой соединительной ткани. Самочувствие пациента зависит от величины площади поражения и наличия или отсутствия осложнений инфаркта миокарда.
В целом, состояние нормализуется. Болевых ощущений в сердце нет либо имеется стабильная стенокардия определенного функционального класса. Человек привыкает к новым условиям жизни.
Диагностика
Электрокардиография — важнейший метод диагностики инфаркта миокарда (ИМ), позволяющий:
— выявить ИМ;
— установить локализацию ИМ, его глубину и распространенность;
— диагностировать осложнения ИМ (аритмии, формирование аневризмы сердца)
ЭКГ при ИМ формируется под влиянием трех зон, образующихся в области инфаркта и представленных в таблице ниже (Bayley)
| Зона некроза — в центре очага поражения | Трансмуральный ИМ | Патологический зубец Q |
| Нетрансмуральный ИМ | Отсутствие или невыраженность патологического зубца Q | |
| Зона повреждения — к периферии от зоны некроза, окружает ее | Субэндокардиальный ИМ | Депрессия сегмента ST |
| Субэпикардиальный или трансмуральный ИМ | Элевация сегмента ST | |
| Зона ишемии — кнаружи от зоны повреждения | Субэндокардиальный ИМ | Высокий и широкий зубец Т (высокий коронарный зубец Т) |
| Субэпикардиальный илитрансмуральный ИМ | Отрицательный симметричный зубец Т с заостренной вершиной (отрицательный коронарный зубец Т) |
Диагностика стадии ИМ (в динамике)
| Стадия ИМ | Наличие зон ИМ | Вид на ЭКГ (для трансмурального ИМ) | ЭКГ-критерии |
| Острейшая стадия (минуты-часы) | Вначале имеется только зона ишемии |  |
Высокий заостренный коронарный зубец Т |
| Затем появляется зона повреждения | Куполообразное смещение сегмента ST кверху от изолинии и его слияние с зубцом Т | ||
| Острая стадия (часы-дни) | Все три зоны поражения: а) зона ишемии |
 |
Начальное формирование зубца Т |
| б) зона повреждения | Куполообразное смещение сегмента ST кверху от изолинии | ||
| в) зона некроза | Наличие патологического зубца Q. Уменьшение величины зубца R. | ||
| Подострая стадия (дни) | Характерно наличие двух зон: а) зона некроза |
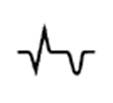 |
Возвращение сегмента ST на уровень изолинии. Наличие патологического зубца Q или QS. |
| б) зона ишемии | Отрицательный симметричный (коронарный) зубец Т с постепенно уменьшающейся глубиной | ||
| Рубцовая стадия (месяцы-годы) | Только сформированный рубец в зоне некроза | 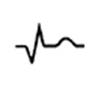 |
Сохранение патологического зубца Q Интервал ST на изолинии Отсутствие динамики зубца Т (остается отрицательным, изоэлектрическим (сглаженным) или слабоположительным) |
Топическая диагностика (локализация) ИМ
В таблице знаком (+) обозначено смещение вверх сегмента RS-Т или положительный зубец Т, знаком (–) — смещение сегмента RS-Т вниз от изолинии или отрицательный зубец Т.
| Локализация ИМ | Отведения | Характер изменений ЭКГ |
| Переднеперегородочный | V1-V3 | 1) Q или QS 2) +(RS-T) 3) -Т |
| Передневерхушечный | V3,V4 | 1) Q или QS 2) +(RS-T) 1) -Т |
| Переднебоковой | I, aVL, V5, V6 | 1) Q 2) +(RS-T) 3) -Т |
| Распространенный передний | I, aVL, V1-V6 | 1) Q или QS 2) +(RS-T) 3) -Т |
| III, aVF | Реципрокные изменения: 1) -(RS-T) 2) + Т (высокие) |
|
| Высокий передний (переднебазальный) | V24-V26, V34- V36 | 1) Q или QS 2) +(RS-T) 3) -Т |
| Заднедиафрагмальный (нижний) | III, aVF или III, II, aVF | 1) Q или QS 2) + (RS-T) 3) -T |
| V1-V4 | Реципрокные изменения: 1) — |
|
| Заднебазальный | V7–V9 (не всегда) | 1) Q или QS 2) +(RS-T) 3) -Т. |
| V1– V3 | Реципрокные изменения: 1) -(RS-T), 2) +Т (высокие); 3) Увеличение R. |
|
| Заднебоковой | V5, V6, Ill, aVF | 1) Q 2) +(RS-T) 3) -Т |
| V1-V3 | Реципрокные изменения: 1) увеличение R 2) -(RS-T) 3) + T (высокие). |
|
| Распространенный задний | III, aVF, III, V5, V6, V7-9 | 1) Q или QS 2) +(RS-T) 3) -Т |
| V1-V3 | Реципрокные изменения: 1) увеличение R 2) -(RS-T) 3) +T (высокие). |
Прекардиальное электрокардиографическое картирование сердца
Исследование применяется при остром инфаркте миокарда передней и переднебоковой стенок левого желудочка для косвенного определения размеров зоны некроза и периинфарктной зоны (участок ишемического повреждения). С этой целью после регистрации ЭКГ с 35 точек на поверхности грудной клетки строят картограмму, состоящую из 35 квадратов, каждый из которых соответствует одному из 35 отведений.
Размеры зоны некроза условно оценивают по количеству отведений, в которых выявляются признаки трансмурального некроза – комплекс QS. Это так называемая «площадь трансмурального некроза» (AQS).
Параметры определения величины периинфарктной зоны:
1. Количество отведений (квадратов), в которых регистрируется подъем сегмента RS-Т выше изолинии. Это площадь RS-T (ARS-T).
2. Величина суммарного подъема сегмента RS-Т во всех отведениях (квадратах) картограммы, в которых фиксируется ишемическое повреждение миокарда (ERS-Т).
3. Значение среднего индивидуального подъема сегмента RS-T (NRS-T), который рассчитывается по формуле: NRS – T= ERS – T/ARS–T
Указанные картографические показатели с успехом используются для наблюдения за динамикой зон некроза и периинфарктной зоны в процессе лечения больных острым инфарктом миокарда, а также для оценки прогноза заболевания; чем выше все описанные показатели, тем больше площадь и глубина поражения миокарда и, соответственно, тем хуже прогноз заболевания.
Коронарография
«Золотой стандарт» диагностики ишемической болезни сердца (ИБС). Больные с многососудистым поражением или поражением ствола левой венечной артерии имеют более высокий риск сердечно-сосудистых событий. Роль коронарографии в оценки критичности бляшки и других повреждений исключительно важна, если предполагается последующая реваскуляризация .
Сложные стенозы, бифуркационные поражения и извитость стенозированных сосудов служат показателями высокого риска. Самый высокий риск имеется при дефектах наполнения, так как при этом существуют внутрисосудистые тромбы. У 10-15% пациентов с болью в груди нет поражения венечных артерий и у них диагноз ИБС исключается.
Компьютерная томография
В настоящее время данное исследование не может заменить коронарографию при остром коронарном синдроме из-за субоптимальной диагностической точности.
КТ сердца не является оптимальным методом диагностики у больных с острым коронарным синдром из-за высокой вероятности в необходимости выполнения коронарной ангиопластики со стентированием. Это обусловлено тем, что на проведение КТ теряется время, пациент получает контрастный препарат и дозу облучения.
Двухмерная ЭхоКГ
Систолическая функция левого желудочка — важный прогностический показатель для больного с ИБС. Регионарные нарушения сократимости могут наступить сразу после ишемии, задолго до некроза, но они неспецифичны для острых событий и могут быть результатом старого инфаркта миокарда.
Транзиторная локальная акинезия и гипокинезия сегментов левого желудочка могут определяться в ходе ишемии, с восстановлением нормальной кинетики стенки при прохождении ишемии.
Отсутствие нарушений локальной сократимости исключает наличие ИМ.
ЭхоКГ имеет ценность для диагностики других причин болей в груди — расслоение и разрыв аорты, гипертрофическая кардиомиопатия , перикардит и массивная ТЭЛА .
Перфузионная сцинтиграфия
Обычно этот метод исследования недоступен, поэтому у острых больных он используется редко. Нормальная сцинтиграмма миокарда с 99Th в покое достоверно исключает крупноочаговый ИМ. Однако ненормальная сцинтиграмма не указывает на острый ИМ, если только нет данных, что раньше сцинтиграмма была нормальной, до наступления острого состояния, но она указывает на наличие ИБС и необходимость дальнейшего обследования.
Магнитно-резонансная томография
МРТ сердца еще пока не стала рутинной процедурой для визуализации венечных сосудов, но позволяет получить информацию о регионарной сократимости, перфузии и жизнеспособности миокарда. Это позволяет идентифицировать больных с ОКС и острым ИМ. Кроме того, МРТ может исключить или подтвердить другие причины боли в груди — миокардит, перикардит , расслаивающую аневризму аорты и ТЭЛА
Лабораторная диагностика
Лабораторное подтверждение острого инфаркта миокарда (ОИМ) основано на выявлении:
— неспецифических показателей тканевого некроза и воспалительной реакции миокарда;
— гиперферментемии (входит в классическую триаду признаков ОИМ: болевой синдром, типичные изменения ЭКГ, гиперферментемия).
Неспецифические показатели тканевого некроза и воспалительной реакции миокарда:
1. Лейкоцитоз, не превышающий обычно 12-15*10 9 /л (выявляются обычно к концу первых суток от начала заболевания и при неосложненном течении инфаркта сохраняются примерно в течение недели).
2. Анэозинофилия.
3. Небольшой палочкоядерный сдвиг формулы крови влево.
4. Увеличение СОЭ (увеличивается обычно спустя несколько дней от начала заболевания и может оставаться повышенной на протяжении 2-3 недель и дольше даже при отсутствии осложнений ИМ).
Правильная трактовка этих показателей возможна только при сопоставлении с клинической картиной заболевания и данными ЭКГ.
Длительное сохранение (более 1 недели) лейкоцитоза или/и умеренной лихорадки у больных ОИМ свидетельствует о возможном развитии осложнений: (пневмония, плеврит Плеврит — воспаление плевры (серозная оболочка, покрывающая легкие и выстилающая стенки грудной полости)
, перикардит, тромбоэмболия мелких ветвей легочной артерии и другие).
Гиперферментемия
Основной причиной повышения активности и содержания ферментов в сыворотке крови у больных ОИМ является разрушение кардиомиоцитов и выход высвобождающихся клеточных ферментов в кровь.
Наиболее ценным для диагностики ОИМ является определение активности нескольких ферментов в сыворотке крови:
— креатинфосфокиназы (КФК) и особенно ее МВ-фракции (МВ-КФК);
— лактатдегидрогеназы (ЛДГ) и ее изофермента 1 (ЛДГ1);
— аспартатаминотрансферазы (АСТ);
— тропонина;
— миоглобина.
Повышение активности МВ-фракции КФК, содержащейся преимущественно в миокарде, специфично для повреждения сердечной мышцы, в первую очередь, для ОИМ. МВ-фракция КФК не реагирует на повреждение скелетных мышц, головного мозга и щитовидной железы.
Динамика МВ-КФК при ОИМ:
— через 3-4 часа активность начинает возрастать;
— через 10-12 часов достигает максимума;
— через 48 часов от начала ангинозного приступа возвращается к исходным цифрам.
Степень повышения активности МВ-КФК в крови в целом хорошо коррелирует с размером ИМ — чем больше объем поражения сердечной мышцы, тем выше активность МВ-КФК 1 .
Динамика КФК при ОИМ:
— к концу первых суток уровень фермента в 3-20 раз превышает норму;
— через 3-4 суток от начала заболевания возвращается к исходным значениям.
1 Следует помнить, что любые кардиохирургические вмешательства (включая коронароангиографию, катетеризацию полостей сердца и электроимпульсную терапию), как правило, сопровождаются кратковременным подъемом активности МВ-фракции КФК.
В литературе имеются также указания на возможность повышения уровня МВ-КФК при тяжелой пароксизмальной тахиаритмии, миокардитах и длительных приступах стенокардии покоя, расцениваемых как проявление нестабильной стенокардии.
В ряде случаев при обширных инфарктах миокарда вымывание ферментов в общий кровоток замедлено, поэтому абсолютное значение активности МВ-КФК и скорость его достижения могут оказаться меньше, чем при обычном вымывании фермента, хотя и в том, и в другом случае площадь под кривой “концентрация-время” остается одинаковой.
Лактатдегидрогеназа
Активность ЛДГ при ОИМ нарастает медленнее, чем КФК и МВ-КФК, и дольше остается повышенной 2 .
Динамика ЛДГ при ОИМ:
— через 2-3 суток от начала инфаркта наступает пик активности;
— к 8-14 суткам происходит возвращение к исходному уровню.
2 Следует помнить, что активность общей ЛДГ повышается также при заболеваниях печени, шоке, застойной недостаточности кровообращения, гемолизе эритроцитов и мегалобластной анемии, ТЭЛА, миокардите, воспалении любой локализации, коронароангиографии, электроимпульсной терапии, тяжелой физической нагрузке и т. д.
Изофермент ЛДГ1 более специфичен для поражений сердца, хотя он также присутствует не только в мышце сердца, но и в других органах и тканях, включая эритроциты.
Аспартатаминотрансфераза
Динамика АСТ при ОИМ:
— через 24-36 часов от начала инфаркта относительно быстро наступает пик повышения активности;
— через 4-7 суток концентрация АСТ возвращается к исходному уровню.
Изменение активности АСТ неспецифично для ОИМ: уровень АСТ вместе с активностью АЛТ повышается при многих патологических состояниях, в том числе при заболеваниях печени 3 .
3 При поражениях паренхимы печени в большей степени возрастает активность АЛТ, а при заболеваниях сердца в большей степени возрастает активность АСТ. При ИМ отношение АСТ/АЛТ (коэффициент де Ритиса) больше 1,33, а при заболеваниях печени отношение АСТ/АЛТ меньше 1,33.
Тропонин
Тропонин представляет собой универсальную для поперечно-полосатой мускулатуры структуру белковой природы, локализующуюся на тонких миофиламентах сократительного аппарата миокардиоцита.
Сам тропониновый комплекс состоит из трех компонентов:
— тропонин С — ответственный за связывание кальция;
— тропонин Т — предназначен для связывания тропомиозина;
— тропонина I — предназначен для ингибирования выше указанных двух процессов.
Тропонин Т и I существуют в специфичных для миокарда изоформах, отличающихся от изоформ скелетных мышц, чем и обусловливается их абсолютная кардиоспецифичность 4 .
Динамика тропонинов при ОИМ:
— спустя 4-5 часов после гибели кардиомиоцитов вследствие развития необратимых некротических изменений, тропонин поступает в периферический кровоток и определяются в венозной крови;
— в первые 12-24 часа от момента возникновения ОИМ достигается пик концентрации.
Кардиальные изоформы тропонина длительно сохраняют свое присутствие в периферической крови:
— тропонин I определяется на протяжении 5-7 дней;
— тропонин Т определяется до 14 дней.
Присутствие этих изоформ тропонина в крови пациента выявляется при помощи ИФА ИФА — иммуноферментный анализ — лабораторный иммунологический метод качественного или количественного определения различных соединений, макромолекул, вирусов и пр., в основе которого лежит специфическая реакция антиген-антитело
с использованием специфических антител.
4 Следует помнить, что тропонины не являются ранними биомаркерами ОИМ, поэтому у рано обратившихся больных с подозрением на острый коронарный синдром при отрицательном первичном результате необходимо повторное (через 6-12 часов после болевого приступа) определение содержания тропонинов в периферической крови. В этой ситуации даже незначительное повышение уровня тропонинов свидетельствует о дополнительном риске для больного, поскольку доказано существование четкой корреляции между уровнем возрастания тропонина в крови и размером зоны поражения миокарда.
Многочисленными наблюдениями было показано, что повышенный уровень тропонина в крови больных с острым коронарным синдромом может рассматриваться как достоверный показатель наличия у пациента ОИМ. В то же время низкий уровень тропонина у этой категории больных свидетельствует в пользу постановки более мягкого диагноза нестабильной стенокардии.
Миоглобин
Специфичность миоглобина для диагностики ОИМ примерно такая же, как КФК, но ниже, чем МВ-КФК.
Уровень миоглобина может повышаться в 2-3 раза после внутримышечных инъекций, и диагностически значимым обычно считают повышение в 10 и более раз.
Подъем уровня миоглобина в крови начинается даже раньше, чем повышение активности КФК. Диагностически значимый уровень зачастую достигается уже через 4 часа и в подавляющем большинстве случаев наблюдается через 6 часов после болевого приступа.
Высокая концентрация миоглобина в крови наблюдается только в течение нескольких часов, поэтому, если не повторять анализ каждые 2-3 часа, пик концентрации можно пропустить. Измерение концентрации миоглобина может быть применено только в случаях поступления больных в стационар менее чем через 6-8 часов после начала болевого приступа.
Принципы ферментативной диагностики ОИМ
1. У пациентов, поступивших в течение первых 24 часов после ангинозного приступа, производится определение активности КФК в крови — это следует делать даже в тех случаях, когда по клиническим и электрокардиографическим данным диагноз инфаркта миокарда не вызывает сомнения, так как степень повышения активности КФК информирует врача о размерах инфаркта миокарда и прогнозе.
2. Если активность КФК находится в пределах нормы или повышена незначительно (в 2-3 раза), либо у пациента имеются явные признаки поражения скелетной мускулатуры или головного мозга, то для уточнения диагноза показано определение активности МВ-КФК.
3. Нормальные величины активности КФК и МВ-КФК, полученные при однократном заборе крови в момент поступления больного в клинику, недостаточны для исключения диагноза ОИМ. Анализ необходимо повторить хотя бы еще 2 раза через 12 и 24 часа.
4. Если больной поступил более чем через 24 часа после ангинозного приступа, но меньше чем через 2 недели, и уровень КФК и МВ-КФК нормальный, то целесообразно определить активность ЛДГ в крови (предпочтительнее — отношение активности ЛДГ1 и ЛДГ2), АСТ вместе с АЛТ и расчетом коэффициента де Ритиса.
5. Если ангинозные боли повторяются у больного после госпитализации, то рекомендуется измерять КФК и МВ-КФК сразу после приступа и через 12 и 24 часа.
6. Миоглобин в крови целесообразно определять только в первые часы после болевого приступа, повышение его уровня в 10 раз и больше указывает на некроз мышечных клеток, однако нормальный уровень миоглобина отнюдь не исключает инфаркта.
7. Определение ферментов нецелесообразно у бессимптомных больных с нормальной ЭКГ. Диагноз на основании одной только гиперферментемии ставить все равно нельзя — должны быть клинические и (или) ЭКГ-признаки, указывающие на возможность ИМ.
8. Контроль количества лейкоцитов и величины СОЭ необходимо проводить при поступлении пациента и затем не реже 1 раза в неделю, чтобы не пропустить инфекционные или аутоиммунные осложнения ОИМ.
9. Исследование уровня активности КФК и МВ-КФК целесообразно проводить только в течение 1-2 суток от предположительного начала заболевания.
10. Исследование уровня активности АСТ целесообразно проводить только в течение 4-7 суток от предположительного начала заболевания.
11. Повышение активности КФК, МВ-КФК, ЛДГ, ЛДГ1, АСТ не является строго специфичным для ОИМ, хотя при прочих равных условиях активность МВ-КФК отличается более высокой информативностью.
12. Отсутствие гиперферментемии не исключает развития ОИМ.
Дифференциальный диагноз
1. Аллергический и инфекционно-токсический шок.
Симптомы: загрудинная боль, одышка, падение артериального давления.
Анафилактический шок может возникать при любой лекарственной непереносимости. Начало болезни острое, четко приурочено к причинному фактору (инъекция антибиотика, прививка с целью профилактики инфекционного заболевания, введение противостолбнячной сыворотки и др.). В некоторых случаях заболевание начинается через 5-8 дней от момента ятрогенного вмешательства, развивается по типу феномена Артюса , в котором сердце выступает в роли шок-органа.
Инфекционно-токсический шок с поражением миокарда может возникнуть при любом тяжелом инфекционном заболевании.
Клинически заболевание очень напоминает инфаркт миокарда (ИМ), отличаясь от него по этиологическим факторам. Дифференциация затрудняется в связи с тем, что при аллергическом и инфекционно-аллергическом шоке могут возникать некоронарогенные некрозы миокарда с грубыми изменениями ЭКГ, лейкоцитозом, увеличением СОЭ, гиперферментемией АСТ, ЛДГ, ГБД , КФК, МВ-КФК.
В отличие от типичного ИМ, при данных шоках на ЭКГ не бывает глубокого зубца Q и комплекса QS, дискордантности изменений конечной части.
2. Перикардит (миоперикардит).
Этиологические факторы перикардита: ревматизм, туберкулез, вирусная инфекция (чаще — вирус Коксаки или ECHO), диффузные болезни соединительной ткани; нередко — терминальная ХПН.
При остром перикардите в процесс часто вовлекаются субэпикардиальные слои миокарда.
В типичном варианте при сухом перикардите возникают тупые, давящие (реже — острые) боли в прекордиальной области без иррадиации в спину, под лопатку, в левую руку, свойственные инфаркту миокарда.
Шум трения перикарда регистрируется в те же дни, что и повышение температуры тела, лейкоцитоз, увеличение СОЭ. Шум стойкий, выслушивается в течение нескольких дней или недель.
При ИМ шум трения перикарда кратковременный; предшествует лихорадке и увеличению СОЭ.
Если у больных перикардитом появляется сердечная недостаточность, то она правожелудочковая или бивентрикулярная. Для ИМ характерна левожелудочковая сердечная недостаточность.
Дифференциально-диагностическая ценность энзимологических тестов невелика. Вследствие поражения субэпикардиальных слоев миокарда у больных перикардитом может регистрироваться гиперферментемия АСТ, ЛДГ, ЛДГ1, ГБД , КФК и даже изоэнзима МВ-КФК.
В правильной постановке диагноза помогают данные ЭКГ. При перикардите имеются симптомы субэпикардиального повреждения в виде элевации интервала ST во всех 12 общепринятых отведениях (нет дискордантности, свойственной ИМ). Зубец Q при перикардите, в отличие от ИМ, не выявляется. Зубец Т при перикардите может быть отрицательным, он становится положительным через 2-3 недели от начала болезни.
При появлении перикардиального экссудата очень характерной становится рентегнологическая картина.
3. Левосторонняя пневмония.
При пневмонии могут появляться боли в левой половине грудной клетки, иногда интенсивные. Однако в отличие от прекордиальных болей при ИМ, они четко связаны с дыханием и кашлем, не имеют типичной для ИМ иррадиации.
Для пневмонии характерен продуктивный кашель. Начало болезни (озноб, повышение температуры, бои в боку, шум трения плевры) совершенно не типично для ИМ.
Физикальные и рентгенологические изменения в легких помогают диагностировать пневмонию.
ЭКГ при пневмонии может меняться (низкий зубец Т, тахикардия), но никогда не бывает изменений, напоминающих таковые при ИМ.
Как и при ИМ, при пневмонии можно обнаружить лейкоцитоз, увеличение СОЭ, гиперферментемию АСТ, ЛДГ, но только при поражении миокарда повышается активность ГБД , ЛДГ1, МВ-КФК.
4. Спонтанный пневмоторакс.
При пневмотораксе возникают сильная боль в боку, одышка, тахикардия. В отличие от ИМ, спонтанный пневмоторакс сопровождается тимпаническим перкуторным тоном на стороне поражения, ослаблением дыхания, рентгенологическими изменениями (газовый пузырь, коллапс легкого, смещение сердца и средостения в здоровую сторону).
Показатели ЭКГ при спонтанном пневмотораксе либо нормальные, либо выявляется преходящее снижение зубца Т.
Лейкоцитоза, увеличения СОЭ при пневмотораксе не бывает. Активность сывороточных ферментов нормальная.
5. Ушиб грудной клетки.
Как и при ИМ возникают сильные боли в груди, возможен шок. Сотрясение и ушиб грудной клетки приводят к повреждению миокарда, что сопровождается элевацией или депрессией интервала ST, негативизацией зубца Т, а в тяжелых случаях — даже появлением патологического зубца Q.
В постановке правильного диагноза решающую роль играет анамнез.
Клиническая оценка ушиба грудной клетки с изменениями ЭКГ должна быть достаточно серьезной, поскольку в основе этих изменений лежат некоронарогенные некрозы миокарда.
6. Остеохондроз грудного отдела позвоночника с компрессией корешка.
При остеохондрозе с корешковым синдромом боли в грудной клетке слева могут быть очень сильными, нестерпимыми. Но, в отличие от болей при ИМ, они исчезают, когда больной принимает неподвижное вынужденное положение, и резко усиливаются при поворотах туловища и дыхании.
Нитроглицерин, нитраты при остеохондрозе совершенно не эффективны.
При грудном «радикулите» определяется четкая локальная болезненность в паравертебральных точках, реже по ходу межреберий.
Количество лейкоцитов, а также значения СОЭ, энзимологических показателей, ЭКГ в пределах нормы.
7. Опоясывающий лишай.
Клиника опоясывающего лишая весьма напоминает описанную выше (см. описание симптомов корешкового синдрома при остеохондрозе позвоночника в грудном отделе).
У некоторых больных может регистрироваться лихорадка в сочетании с умеренным лейкоцитозом, увеличением СОЭ.
ЭКГ, ферментные тесты, как правило, часто помогают исключить диагноз ИМ.
Диагноз «опоясывающий лишай» становится достоверным со 2-4 дня болезни, когда по ходу межреберий появляется характерная пузырьковая (везикулярная) сыпь.
8. Бронхиальная астма.
Астматический вариант ИМ в чистом виде встречается редко, чаще удушье сочетается с болями в предсердечной области, аритмией, симптомами шока.
9. Острая левожелудочковая недостаточность осложняет течение многих болезней сердца, в числе которых кардиомиопатии, клапанные и врожденные пороки сердца, миокардиты и другие.
10. Острый холецистопанкреатит.
При остром холецистопанкреатите, как и при гастралгическом варианте ИМ, возникают сильные боли в эпигастральной области, сопровождающиеся слабостью, потливостью, гипотензией. Однако боли при остром холецистопанкреатите локализуются не только в эпигастрии, но и в правом подреберье, иррадиируют вверх и вправо, в спину, иногда могут быть опоясывающими. Характерно сочетание болей с тошнотой, рвотой, причем в рвотных массах определяется примесь желчи.
Пальпаторно определяется болезненность в точке желчного пузыря, проекции поджелудочной железы, положительные симптом Кера , симптом Ортнера , симптом Мюсси , что не характерно для ИМ.
Вздутие живота, локальное напряжение в правом верхнем квадранте не типично для ИМ.
Лейкоцитоз, увеличение СОЭ, гиперферментемия АСТ, ЛДГ могут появляться при обоих заболеваниях. При холецистопанкреатите отмечается увеличение активности альфа-амилазы сыворотки крови и мочи, ЛДГ 3-5. При ИМ следует ориентироваться на высокие показатели ферментной активности КФК, МВ-КФК, ГБД .
ЭКГ при остром холецистопанкреатите: снижение интервала ST в ряде отведений, слабо отрицательный или двухфазный зубец Т.
Крупноочаговое метаболическое повреждение миокарда существенно ухудшает прогноз панкреатита, нередко является ведущим фактором в летальном исходе.
11. Прободная язва желудка.
Как при ИМ, характерны острые боли в эпигастрии. Однако при прободной язве желудка отмечаются нестерпимые, «кинжальные» боли, максимально выраженные в момент прободения и затем уменьшающиеся в интенсивности, при этом эпицентр болей смещается несколько вправо и вниз.
При гастралгическом варианте ИМ боли в эпигастрии могут быть интенсивными, но для них не характерно столь острое, мгновенное начало с последующим спадом.
При прободной язве желудка через 2-4 часа от момента прободения симптоматика меняется. У больных с прободной гастродуоденальной язвой появляются симптомы интоксикации; язык становится сухим, черты лица заостряются; живот становится втянутым, напряженным; отмечаются положительные симптомы раздражения; перкуторно определяется «исчезновение» печеночной тупости; рентгенологически выявляется воздух под правым куполом диафрагмы.
Как при ИМ, так и при прободении язвы температура тела может быть субфебрильной, отмечается умеренный лейкоцитоз в течение первых суток.
Для ИМ типично увеличение активности сывороточных ферментов (ЛДГ, КФК, МВ КФК).
ЭКГ при прободной язве желудка в течение первых суток, как правило, не меняется. На следующий день возможны изменения конечной части за счет электролитных нарушений.
12. Рак кардиального отдела желудка.
При раке кардии нередко возникают интенсивные давящие боли в эпигастрии и под мечевидным отростком, сочетающиеся с транзиторной гипотонией.
В отличие от ИМ при раке кардии эпигастральные боли закономерно повторяются ежедневно, они связаны с приемом пищи.
СОЭ увеличивается при обоих заболеваниях, однако динамика активности ферментов КФК, МВ КФК, ЛДГ, ГБД характерна только для ИМ.
Для исключения гастралгического варианта ИМ необходимо ЭКГ-исследование. На ЭКГ выявляются изменения интервала ST (чаще депрессия) и зубца Т (изоэлектричный или слабо отрицательный) в III, avF отведениях, что служит поводом для диагностики мелкоочагового заднего ИМ.
При раке кардии ЭКГ «застывшая», на ней не удается определить характерной для ИМ динамики.
Диагноз рака уточняется при проведении ФГДС , рентгенологического исследования желудка в различных положениях тела исследуемого, в том числе и в положении антиортостаза.
13. Пищевая токсикоинфекция.
Как и при ИМ появляются боли в эпигастрии, падает артериальное давление. Однако при пищевой токсикоинфекции боль в эпигастрии сопровождается тошнотой, рвотой, гипотермией. Диарея не всегда встречается при пищевой токсикоинфекции, но ее никогда не бывает при ИМ.
ЭКГ при пищевой токсикоинфекции либо не меняется, либо во время исследования определяются «электролитные нарушения» в виде корытообразного смещения вниз интервала ST, слабоотрицательного или изоэлектрического зубца Т.
Лабораторные исследования при пищевой токсикоинфекции показывают умеренный лейкоцитоз, эритроцитоз (сгущение крови), небольшое повышение активности АЛТ, АСТ, ЛДГ без существенных изменений активности КФК, МВ-КФК, ГБД , свойственных ИМ.
14. Острое нарушение мезентерального кровообращения.
Боль в эпигастрии, падение артериального давления возникают при обоих заболеваниях. Дифференциация усложняется тем, что тромбоз мезентеральных сосудов, как и ИМ, поражает, как правило, людей пожилого возраста с различными клиническим проявлениями ИБС, с артериальной гипертонией.
При нарушении кровообращения в системе мезентеральных сосудов боли локализуются не только в эпигастрии, но и по всему животу. Живот умеренно вздут, аускультативно не выявляются звуки перистальтики кишечника, возможно обнаружение симптомов раздражения брюшины.
Для уточнения диагноза проводится обзорная рентгенография брюшной полости и определяется наличие или отсутствие перистальтики кишечника и скопления газа в кишечных петлях.
Нарушение мезентерального кровообращения не сопровождается изменениями ЭКГ и ферментных показателей, характерных для ИМ.
При затруднении в диагностике тромбоза мезентеральных сосудов патогномоничные изменения могут быть обнаружены при лапароскопии и ангиографии.
15. Расслаивающая аневризма абдоминального отдела аорты.
При абдоминальной форме расслаивающей аневризмы аорты в отличие от гастралгического варианта ИМ, характерны следующие признаки:
— начало болезни с болей в груди;
— волнообразный характер болевого синдрома с иррадиацией в поясницу по ходу позвоночника;
— появление опухолевидного образования эластичной консистенции, пульсирующего синхронно с сердцем;
— появление систолического шума над опухолевидным образованием;
— нарастание анемии.
16. Некоронарогенные некрозы миокарда могут возникать при тиреотоксикозе, лейкозах и анемиях, системных васкулитах, гипо- и гипергликемических состояниях.
Клинически на фоне симптоматики основной болезни отмечаются боли в сердце (временами сильные), одышка.
Данные лабораторных исследований бывают малоинформативными в дифференциации некоронарогенных некрозов с ИМ атеросклеротического генеза. Гиперферментемия ЛДГ, ЛДГ1, ГБД , КФК, МВ-КФК обусловлены миокардиальными некрозами как таковыми, вне зависимости от их этиологии.
На ЭКГ при некоронарогенных некрозах миокарда выявляются изменения конечной части – депрессия или, реже, элевация интервала ST, негативные зубцы Т, с последующей динамикой, соответствующей нетрансмуральному ИМ.
Точный диагноз устанавливается на основе всей симптоматики заболеваний. Только такой подход дает возможность методически правильно оценить собственно сердечную патологию.
18. Опухоли сердца (первичные и метастатические).
При опухолях сердца могут появляться упорные интенсивные боли в прекордиальной области, резистентные к нитратам, сердечная недостаточность, аритмии.
На ЭКГ отмечаются патологический зубец Q, элевация интервала ST, отрицательный зубец Т. В отличие от ИМ при опухоли сердца не бывает типичной эволюции ЭКГ, она малодинамична.
Сердечная недостаточность, аритмии рефрактерны к лечению. Диагноз уточняется при тщательном анализе клинико-рентгенологических и Эхо-КГ-данных.
19. Посттахикардиальный синдром.
Посттахикардиальным синдромом называется ЭКГ-феномен, выражающийся в преходящей ишемии миокарда (депрессия интервала ST, негативный зубец Т) после купирования тахиаритмии. Данный симптомокомплекс необходимо оценивать очень осторожно.
Во-первых, тахиаритмия может быть началом ИМ и ЭКГ после ее купирования зачастую лишь выявляет инфарктные изменения.
Во-вторых, приступ тахиаритмии в такой степени нарушает гемодинамику и коронарный кровоток, что он может приводить к развитию миокардиальных некрозов, особенно при изначально дефектном коронарном кровообращении у больных со стенозирующим коронарным атеросклерозом. Следовательно, диагноз посттахикардиального синдрома достоверен после тщательного наблюдения за больным с учетом динамики клинических, ЭхоКГ-, лабораторных данных.
20. Синдром преждевременной реполяризации желудочков.
Синдром выражается в элевации интервала ST в вильсоновских отведениях, начинающегося с точки J, расположенной на нисходящем колене зубца R.
Этот синдром регистрируется у здоровых людей, спортсменов, больных с нейроциркуляторной дистонией.
Для постановки правильного диагноза надо знать о существовании ЭКГ-феномена — синдрома преждевременной реполяризации желудочков. При этом синдроме отсутствует клиника ИМ, не бывает свойственной ему динамика ЭКГ.
Примечание
При трактовке симптома «острая боль в эпигастрии» в сочетании с гипотензией при проведении дифференциального диагноза с ИМ надо иметь в виду и более редкие болезни: острую надпочечниковую недостаточность; разрыв печени, селезенки или полого органа при травме; сифилитическую сухотку спинного мозга с табетическими желудочными кризами (анизокория, птоз, рефлекторная неподвижность глазных яблок, атрофия зрительного нерва, атаксия, отсутствие коленных рефлексов); абдоминальные кризы при гипергликемии, кетоацидозе у больных с сахарным диабетом.
Осложнения
Группы осложнений инфаркта миокарда (ИМ):
1. Электрические — нарушения ритма и проводимости:
— брадитахиаритмии;
— экстрасистолии;
— внутрижелудочковые блокады;
— АВ-блокады.
Данные осложнения практически постоянно встречаются при крупноочаговом ИМ. Часто аритмии не являются угрожающими для жизни, но свидетельствуют о серьезных нарушениях (электролитных, продолжающейся ишемии, вагальной гиперактивности и др.), требующих коррекции.
2. Гемодинамические осложнения:
2.1 Вследствие нарушений насосной функции сердца:
— острая левожелудочковая недостаточность;
— острая правожелудочковая недостаточность;
— бивентрикулярная недостаточность;
— кардиогенный шок;
— аневризма желудочка;
— расширение инфаркта.
2.2 Вследствие дисфункции сосочковых мышц.
2.3 Вследствие механических нарушений:
— острая митральная регургитация вследствие разрыва сосочковых мышц;
— разрывы сердца, свободной стенки или межжелудочковой перегородки;
— аневризмы левого желудочка;
— отрывы сосочковых мышц.
2.4 Вследствие электромеханической диссоциации.
3. Реактивные и прочие осложнения:
— эпистенокардический перикардит;
— тромбоэмболии сосудов малого и большого круга кровообращения;
— ранняя постинфарктная стенокардия;
— синдром Дресслера Дресслера синдром — сочетание перикардита с плевритом, реже пневмонией и эозинофилией, развивающееся на 3-4-й неделе с момента возникновения острого инфаркта миокарда; обусловлено сенсибилизацией организма к деструктивно измененным белкам миокарда
.
По времени появления осложнения ИМ классифицируют на:
1. Ранние осложнения, возникающие в первые часы (нередко на этапе транспортировки больного в стационар) или в острейший период (3-4 дня):
— нарушения ритма и проводимости (90%), вплоть до фибрилляции желудочков и полной АВ-блокады (самые частые осложнения и причина летальности на догоспитальном этапе);
— внезапная остановка сердца;
— острая недостаточность насосной функции сердца — острая левожелудочковая недостаточность и кардиогенный шок (до 25%);
— разрывы сердца — наружные, внутренние; медленнотекущие, одномоментные (1-3%);
— острая дисфункция сосочковых мышц (митральная регургитация);
— ранний эпистенокардический перикардит.
2. Поздние осложнения (возникают на 2-3-й неделе, в период активного расширения режима):
— постинфарктный синдром Дресслера Дресслера синдром — сочетание перикардита с плевритом, реже пневмонией и эозинофилией, развивающееся на 3-4-й неделе с момента возникновения острого инфаркта миокарда; обусловлено сенсибилизацией организма к деструктивно измененным белкам миокарда
(3%);
— пристеночный тромбоэндокардит (до 20%);
— хроническая сердечная недостаточность;
— нейротрофические расстройства (плечевой синдром, синдром передней грудной стенки).
Как на ранних, так и на поздних стадиях течения ИМ могут возникать следующие осложнения:
— острая патология желудочно-кишечного тракта (острые язвы, желудочно-кишечный синдром, кровотечения и др.);
— психические изменения (депрессия, истерические реакции, психоз);
— аневризмы сердца (у 3-20% больных);
— тромбоэмболические осложнения: системные (вследствие пристеночного тромбоза) и ТЭЛА (из-за тромбоза глубоких вен голеней).
Тромбоэмболии клинически выявляются у 5-10% больных (на аутопсии — у 45%). Часто они имеют бессимптомное течение и являются причиной смерти у ряда госпитализированных больных с ИМ (до 20%).
У некоторых пожилых мужчин с доброкачественной гипертрофией предстательной железы развивается острая атония мочевого пузыря (снижается его тонус, нет позывов к мочеиспусканию) с увеличением объема пузыря до 2 л, задержкой мочеиспускания на фоне постельного режима и лечения наркотическими препаратами, атропином.
Лечение
Цели неотложной терапии инфаркта миокарда (ИМ):
— купирование болевого синдрома;
— восстановление коронарного кровотока;
— уменьшение работы сердца и потребности миокарда в кислороде;
— ограничение размеров ИМ;
— лечение и профилактика осложнений ИМ.
Купирование болевого приступа
Морфин — препарат выбора для купирования болевого синдрома при ИМ на догоспитальном этапе. Морфин обладает необходимыми эффектами и достаточной для транспортировки длительностью действия.
Препарат вводится внутривенно дробно: 1 мл 1% раствора разводят физиологическим раствором натрия хлорида до 20 мл (1 мл полученного раствора содержит 0,5 мг активного вещества) и вводят 2-5 мг каждые 5-15 минут до полного устранения болевого синдрома либо до появления побочных эффектов (гипотензии, угнетения дыхания, рвоты).
Суммарная доза не должна превышать 10-15 мг (1-1,5 мл 1% раствора) морфина (на догоспитальном этапе не допускается превышение дозы 20 мг).
При невыраженном болевом синдроме, пациентам старческого возраста и ослабленным больным наркотические анальгетики могут вводиться подкожно или внутримышечно. Не рекомендуется вводить подкожно более 60 мг морфина в течение 12 часов.
Для решения вопроса о возможности использования наркотических анальгетиков необходимо:
— убедиться, что типичный или атипичный болевой синдром не является проявлением “острого живота”, и изменения ЭКГ являются специфическим проявлением ИМ, а не неспецифической реакцией на катастрофу в брюшной полости;
— выяснить, имеются ли в анамнезе хронические заболевания системы дыхания (в частности — бронхиальная астма);
— уточнить, когда было последнее обострение бронхообструктивного синдрома;
— установить, имеются ли в настоящее время признаки дыхательной недостаточности, какие, какова степень ее выраженности;
— выяснить, имеется ли у больного в анамнезе судорожный синдром, когда был последний припадок.
Восстановление коронарного кровотока в острейшей фазе ИМ
Поскольку непосредственной причиной развития ИМ является окклюзия коронарной артерии, в основе лечения лежит восстановление коронарного кровотока — коронарная реперфузия путем системного тромболизиса.
Все больные ИМ должны быть безотлагательно обследованы для уточнения показаний и противопоказаний к восстановлению коронарного кровотока.
Показания к проведению тромболизиса:
1. Наличие подъема сегмента ST более чем на 1 mm по крайней мере в двух стандартных отведениях ЭКГ и более чем на 2 mm в двух смежных грудных отведениях.
2. Остро возникшая полная блокада левой ножки пучка Гиса при сроке, прошедшем с начала заболевания, более 30 минут, но не превышающем 12 часов.
Применение тромболитических средств возможно и позже, в случаях когда сохраняются подъем сегмента ST, продолжается боль и/или наблюдается нестабильная гемодинамика.
Абсолютные противопоказания к тромболитической терапии:
— ранее перенесенный геморрагический инсульт или нарушение мозгового кровообращения неизвестной этиологии;
Инфаркт миокарда (сердечный приступ) — симптомы и лечение
Что такое инфаркт миокарда (сердечный приступ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Колесниченко Ирины Вячеславовны, кардиолога со стажем в 26 лет.
Над статьей доктора Колесниченко Ирины Вячеславовны работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Кардиолог Cтаж — 26 лет Кандидат наук
Городская больница №3
Клиника «Александрия» на Гагарина
Дата публикации 13 ноября 2019 Обновлено 3 августа 2021
Определение болезни. Причины заболевания
Инфаркт миокарда (Myocardial infarction, heart attack) — это развитие некроза (омертвения) сердечной мышцы из-за остро возникшей недостаточности кровотока, при которой нарушается доставка кислорода к сердцу. Может сопровождаться болью в разных частях тела, потерей сознания, тошнотой, потливостью и другими симптомами [5] .
Инфаркт миокарда является одной из наиболее острых клинических форм ишемической болезни сердца (ИБС).
Мужчины болеют инфарктом миокарда значительно чаще (примерно в 5 раз), чем женщины [6] . Эта закономерность особенно выражена в молодом и среднем возрасте. Инфаркты у женщин случаются в среднем на 10-15 лет позже по сравнению с мужчинами. Это может быть связано с более поздним развитием атеросклероза под влиянием защитного действия женских половых гормонов (эстрогенов) и меньшим распространением вредных привычек среди женщин. Заболеваемость инфарктом миокарда значительно увеличивается с возрастом.
Факторы риска развития инфаркта миокарда делятся на три группы:
- Факторы, которые можно скорректировать или устранить: курение, высокий уровень холестерина липопротеинов низкой плотности в крови, артериальная гипертензия.
- Факторы, которые хуже поддаются коррекции: сахарный диабет, снижение уровня липопротеинов высокой плотности (иначе их называют «хорошим холестерином»), ожирение, менопауза и постменопауза, употребление алкоголя, стресс, питание с избыточной калорийностью и высоким содержанием животных жиров, высокое содержание в крови липопротеина (А), высокий уровень гомоцистеина.
- Факторы, которые нельзя скорректировать или устранить: пожилой возраст, мужской пол, наследственность — раннее развитие инфаркта миокарда у родителей или кровных родственников до 55 лет.
Этиологические факторы инфаркта миокарда можно разделить на две группы:
1. Атеросклеротическое поражение сердечных артерий и развитие в них тромбов при разрыве атеросклеротической бляшки.
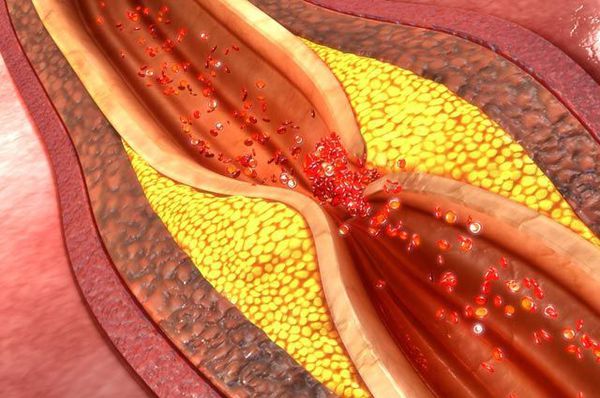
2. Неатеросклеротическое поражение коронарных артерий, возникшее из-за воспалительного процесса в стенках артерий различной этиологии. Воспаление возникает в результате:
- травмы артерии;
- радиационных повреждений (в том числе при лучевой терапии рака),
- снижения коронарного кровотока из-за спазма коронарных артерий, расслоения аорты или коронарной артерии, эмболии (закупорки коронарных сосудов);
- врождённых аномалий коронарных сосудов;
- несоответствия между потребностями миокарда в кислороде и его доставкой;
- нарушения свёртывания крови.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы инфаркта миокарда
Симптоматика инфаркта миокарда зависит от периода развития заболевания: прединфарктного, острейшего, острого, подострого и постинфарктного.
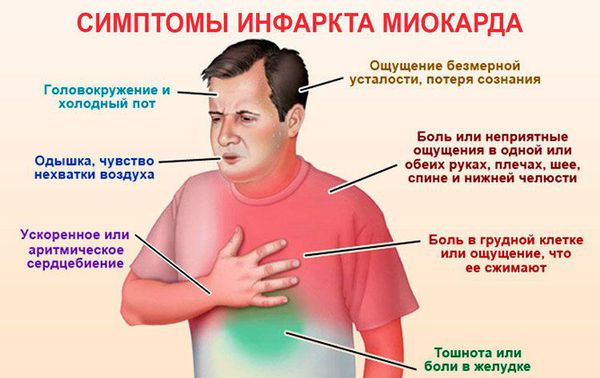
Прединфарктный период инфаркта миокарда. В прединфарктном периоде могут возникать кардиальные (касаются работы сердца) и некардиальные симптомы. К кардиальным сиптомам относятся: боли за грудиной, одышка, сердцебиения, аритмии. К некардиальным — слабость, потливость, головокружения, ощущение тяжести и боли в области желудка (в эпигастрии). В прединфарктном периоде могут наблюдаться только некардиальные симптомы при наличии аритмии и одышки (или без), но сам период проходит без болевых ощущений. При осмотре пациента можно обнаружить небольшой цианоз (посинение) губ, пространства под ногтевыми пластинами, аритмичный пульс, повышение болевой чувствительности кожи в области сердца.
Острейший период инфаркта миокарда. Болевой синдром — самый характерный симптом острейшего периода типичного инфаркта миокарда. У большинства пациентов наблюдаются чрезвычайно интенсивные боли сжимающего, давящего характера. Больные сравнивают давление с обручем или железными клещами, или с тяжёлой плитой, лежащей на груди. Могут ощущаться интенсивные жгучие (пожар в груди, ощущение кипятка, льющегося на грудь) или кинжальные боли. Болезненные ощущения сильнее, чем при обычном приступе стенокардии. Их интенсивность зависит от размера инфаркта миокарда и возраста больного. Тяжёлый и длительный приступ боли чаще наблюдается при обширных инфарктах. Более интенсивные боли наблюдаются у молодых больных по сравнению с лицами пожилого и старческого возраста. Нужно отметить, что слабо выраженные боли при инфаркте миокарда могут быть у больных с сахарным диабетом из-за повреждения вегетативной нервной системы и снижения болевой чувствительности.
Локализация боли:
- за грудиной (чаще всего);
- часто распространяется на прекордиальную зону (слева от края грудины) или на всю переднюю поверхность грудной клетки;
- в загрудинной области и справа от края грудины;
- в подложечной области (эпигастрии).
При осмотре больного кожные покровы бледные, повышена их влажность, отмечается цианоз (посинение) губ, ушей, носа, пространств под ногтями. Может наблюдаться небольшое увеличение частоты дыхания. Часто наблюдается учащение пульса до 90-100 ударов в минуту, однако в начале болевого приступа может возникать непродолжительное урежение ритма сердца (брадикардия), пульс может быть аритмичным.
Боль часто иррадиирует (распространяется) в другие части тела, как правило — в левую руку, иногда в обе, иногда появляется ощущение сильной сжимающей боли в запястьях (симптом «наручников», «браслетов»). Реже отдаёт в левое плечо, левую лопатку, область между лопаток, шею, нижнюю челюсть, ухо, глотку. Совсем редко — в правую руку и другие части тела. Возможны случаи, когда боль воспринимается больным преимущественно в зоне иррадиации, что затрудняет диагностику.
Для инфаркта очень характерен волнообразный характер боли в области сердца. Боль постепенно нарастает, усиливается, иногда становится невыносимой, затем её интенсивность несколько снижается. Однако вскоре боль снова нарастает и становится ещё сильнее. В среднем боли продолжаются несколько десятков минут (всегда больше 20-30 минут), иногда несколько часов, в некоторых случаях в течение одних-двух суток (при увеличении зоны некроза сердечной мышцы).
Во время приступа интенсивной боли при очень сильном возбуждении могут появляться галлюцинации.
В отдельных случаях боль в области сердца может быть не очень интенсивной или даже отсутствовать совсем. У таких больных развиваются атипичные формы инфаркта миокарда, когда на первый план выступает не болевой приступ, а другие проявления (например, аритмии или удушье).
Острый период инфаркта миокарда. В остром периоде окончательно формируется очаг некроза, боль обычно к этому моменту исчезает. Если боль сохраняется, то это может быть связано с расширением зоны инфаркта. Пульс учащённый, артериальное давление снижается.
Атипичные формы инфаркта миокарда. В ряде случаев могут возникать атипичные формы инфаркта миокарда. Они формируются из-за пожилого возраста, развитие инфаркта на фоне тяжело протекающей артериальной гипертензии или сердечной недостаточности, а также у тех, кто уже перенёс инфаркт ранее. Другими факторами являются: повышение порога болевой чувствительности, поражение вегетативной нервной системы с иннервацией (переходом от очага заболевании) боли в сердце (к примеру, при сахарном диабете или у больных алкоголизмом). Симптомы зависят от формы атипично протекающего инфаркта миокарда.
Патогенез инфаркта миокарда
В основе развития инфаркта миокарда лежат три компонента:
1. Разрыв атеросклеротической бляшки.
2. Тромбоз (образование тромба и закупорка им коронарной артерии).
3. Вазоконстрикция (резкое сужение коронарной артерии).
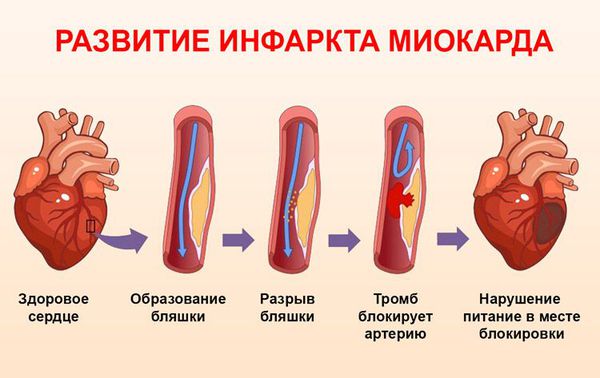
Разрыв атеросклеротической бляшки или эрозия её поверхности происходит следующим образом. В бляшке развивается воспалительная реакция, мощным стимулятором которой является окисление проникающих в неё липопротеинов низкой плотности (одной из вредных фракций холестерина). После чего в бляшку поступают макрофаги (клетки, пожирающие другие вредоносные для организма клетки) и начинают продуцировать ферменты, разрушающие фиброзную покрышку бляшки. Прочность покрышки снижается и происходит разрыв.
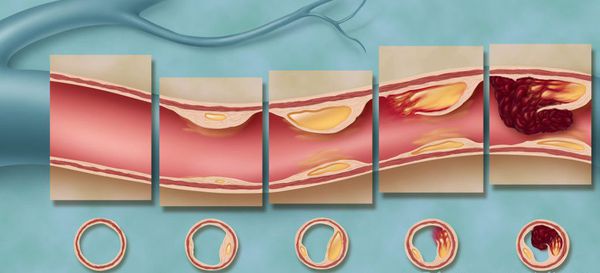
Факторы, провоцирующие надрыв или разрыв атеросклеротической бляшки:
- накопление в бляшке окисленных липопротеинов низкой плотности;
- значительное давление крови на края бляшки;
- выраженный подъём артериального давления;
- курение;
- интенсивная физическая нагрузка.
В области повреждения бляшки происходит прилипание и склеивание тромбоцитов, что приводит к закупорке коронарной артерии. При разрыве бляшки кровь поступает внутрь, взаимодействуя с ядром бляшки. Тромб сначала образуется внутри бляшки, заполняет её объем, а затем распространяется в просвет коронарной артерии. При внезапном полном закрытии просвета коронарной артерии тромбом развивается сквозной инфаркт миокарда — некротизируется (омертвевает) вся толща сердечной мышцы. Сквозной инфаркт миокарда протекает тяжелее и более опасен в плане осложнений и смертельного исхода, чем мелкоочаговый несквозной инфаркт миокарда.
При неполной закупорке коронарной артерии (если тромб растворяется спонтанно или при помощи лекарств) формируется несквозной (нетрасмуральный) инфаркт миокарда.

В развитии закупорки просвета коронарной артерии большую роль играет спазм артерии, который обусловлен нарушением функции эндотелия, влиянием сосудосуживающих веществ, которые выделяют тромбоциты во время образования тромба. В итоге это приводит к спазму артерий, а тромбоциты начинают склеиваться ещё активней.
Развитие спазма коронарных артерий увеличивает степень её закупорки, вызванной атеросклеротической бляшкой и тромбом. Ток крови прекращается, что вызывает некроз миокарда [6] [7] .
Классификация и стадии развития инфаркта миокарда
Инфаркт миокарда можно классифицировать следующим образом [6] :
1. По глубине и обширности некроза на основе данных ЭКГ:
1.1. Крупноочаговый (обширный) QS или Q-инфаркт (ИМ с патологическим зубцом QS и Q на ЭКГ):
- крупноочаговый трансмуральный (т.е. сквозь всю стенку миокарда) (ИМ с патологическим зубцом QS);
- крупноочаговый нетрансмуральный (ИМ с патологическим зубцом Q).
1.2. Мелкоочаговый «не Q»инфаркт миокарда (без патологического зубца Q):
- субэндокардиальный (очаг некроза располагается только во внутренних субэндокардиальных слоях стенки сердца);
- интрамуральный (очаг некроза расположен в средних мышечных слоях стенки сердца).
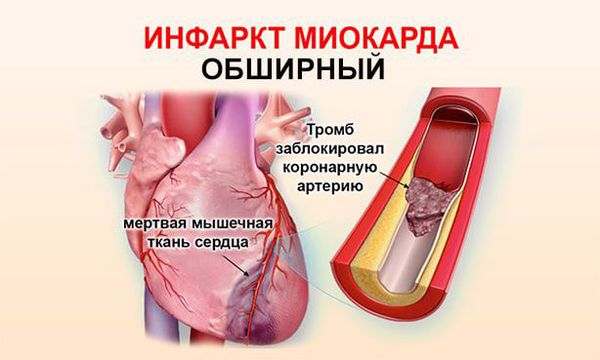
2. По локализации инфаркта миокарда:
- инфаркт левого желудочка: передний; переднеперегородочный; верхушечный; переднебоковой; боковой; задний; заднебоковой; передне-задний;
- инфаркт миокарда правого желудочка;
- инфаркт миокарда предсердий.
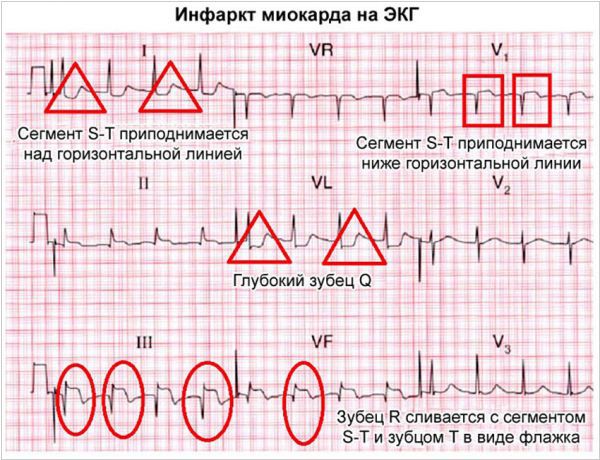
3. По периодам развития инфаркта:
- прединфарктный (продромальный) — период нарастания тяжести уже имеющейся у пациента ишемической болезни сердца; продолжается от нескольких часов до 1-го месяца, наблюдается у 70-80% больных; одним из вариантов этого периода могут быть впервые возникшая стенокардия или рецидив стенокардии после длительного безболевого периода; наблюдается у больных после ранее перенесенного инфаркта или аорто-коронарного шунтирования; возможен безболевой вариант продромального периода;
- острейший — от момента возникновения недостаточного кровоснабжения миокарда до начала формирования очага некроза сердечной мышцы; продолжительность колеблется от 30 минут до 2-х часов (максимально до четырёх часов); опасен в плане возникновения жизнеугрожающих осложнений;
- острый — окончательно образуется очаг некроза, в нем формируется миомаляция (размягчение некротизированной мышечной ткани); продолжается от 2 до 14 дней, опасен в плане возникновения жизнеугрожающих осложнений;
- подострый — формируется полные замещение некротических масс молодой соединительной тканью, образующейся при процессах заживления дефектов в различных тканях и органах, на фоне очага некроза формируется рубец из соединительной ткани; длительность колеблется от 6 до 8 недель при неосложнённом инфаркте в зависимости от размера зоны некроза, возраста больного, а также наличия или отсутствия осложнений;
- постинфарктный (ближайший — 2-6 месяцев, отдалённый — после полугода) — на месте некроза миокарда полностью формируется рубец из соединительной ткани; сердечно-сосудистая система максимально полно адаптируется к новым условиям функционирования, когда омертвевший зарубцевавшийся участок сердечной мышцы выключается из сократительной функции.
4. По особенностям клинического течения:
- затяжное течение, рецидивирование, повторный инфаркт миокарда;
- неосложнённый инфаркт миокарда; инфаркт миокарда с осложнениями;
- типичное течение (классический вариант), атипичный инфаркт миокарда.
Осложнения инфаркта миокарда
Осложнения при инфаркте усугубляют течение заболевания и определяют его прогноз. Чаще всего встречаются следующие осложнения:
- Нарушения сердечного ритма и проводимости. Наблюдаются у 90-95 % больных в первые сутки после инфаркта. За такими нарушениями важно следить, так как они способны привести к смерти. Тяжёлые аритмии (например приступообразная желудочковая тахикардия) могут провоцировать развитие сердечной недостаточности. Степень выраженности и характер нарушений зависят от обширности, глубины, локализации инфаркта миокарда, а также от предшествующих заболеваний. Возможно возникновение аритмий сердца даже после восстановления кровотока (возникают так называемые «реперфузионные аритмии») [9] .
- Острая сердечная недостаточность. К развитию острой сердечной недостаточности приводят обширные, сквозные инфаркты. Наиболее тяжёлая степень острой сердечной недостаточности левого желудочка проявляется сердечной астмой и отёком лёгких. Возникает выраженное удушье, ощущение нехватки воздуха, сильное чувство страха смерти. Больной ведёт себя беспокойно, судорожно хватает ртом воздух, находится в вынужденном полувозвышенном или сидячем положении. Дыхание частое, поверхностное. При прогрессировании недостаточности появляются кашель с отделением пенистой розовой мокроты и «клокочущее» дыхание, на расстоянии слышны влажные хрипы (симптом «кипящего самовара»). Симптомы указывают на развитие отёка лёгких. При прогрессировании левожелудочковой недостаточности и присоединении недостаточности правого желудочка у больного появляются чувство тяжести и боль в правом подреберье, что связано с острым набуханием печени. Видно набухание шейных вен, которое усиливается при надавливании на увеличенную печень. Появляется отёчность голеней и стоп.
- Кардиогенный шок. Развивается при крайней степени левожелудочковой недостаточности, из-за которой снижается сократительная функция миокарда. Это не компенсируется повышением тонуса сосудов и приводит к нарушению кровоснабжения всех органов и тканей, прежде всего жизненно важных. Систолическое артериальное давление падает до 80-70-ти мм рт. ст. и ниже [5] .
- Аневризма левого желудочка. Это ограниченное выбухание тканей сердца, которые подверглись размягчению, истончению и потеряли сократительную способность. Из-за аневризмы определённый объём крови выключается из циркуляции. Постепенно на этом фоне может развиться сердечная недостаточность. При аневризме сердца могут развиваться тромбоэмболические осложнения. Часто возникают приступообразные нарушения ритма. Опасность заключается ещё и в том, что аневризма может расслоиться и разорваться.
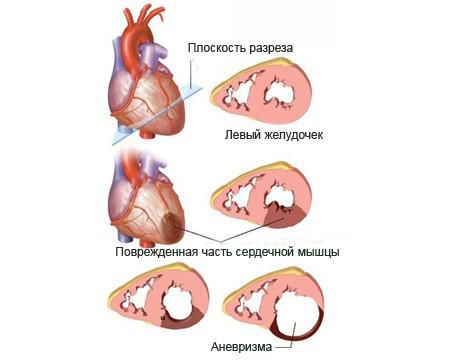
- Ранняя постинфарктная стенокардия. Это частые приступы стенокардии напряжения и покоя, возникающие в госпитальном периоде. Иногда может развиваться при недостаточном растворении тромба с помощью тромболитической терапии. При стенокардии прогноз неблагоприятный, так как она может предвещать рецидив инфаркта и даже внезапную смерть.
- Перикардит. Воспаление наружной оболочки сердца наблюдается при сквозном и обширном инфаркте. При перикардите, как правило, прогноз благоприятен.
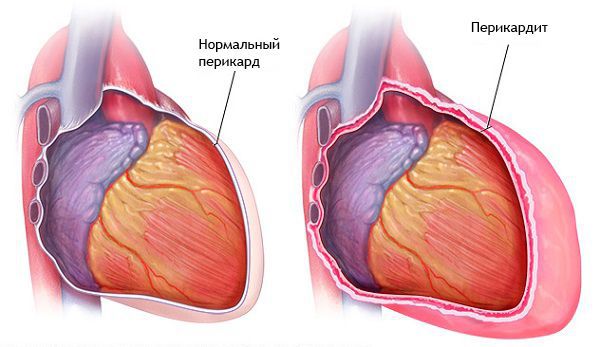
- Тромбоэмболические осложнения. Закупорка кровеносного сосуда тромбом может произойти из-за повышения свёртывающей активности крови, атеросклеротического поражения артерий, тромбоза в зоне инфаркта миокарда, наличия тромба в аневризме левого желудочка. Возникновению тромбоэмболических осложнений способствуют воспаления внутренней оболочки стенок вен нижних конечностей, длительный постельный режим и выраженная недостаточность кровообращения. Важно отметить, что в связи с активным применением терапии, направленной на растворение тромба, тромбоэмболии возникают нечасто, всего лишь у 2-6 % больных.
- Тромбоэндокардит. Это асептическое (без участия микробов) воспаление внутренней стенки сердца с образованием пристеночных тромбов в области некроза.
- Нарушения мочеиспускания. После инфаркта может возникнуть значительное снижение тонуса мочевого пузыря и задержка мочеиспускания. Наиболее часто это имеет место в первые дни заболевания у мужчин пожилого возраста с доброкачественной гиперплазией (увеличением) предстательной железы. Появляются жалобы на невозможность помочиться, ощущение переполненности мочевого пузыря и боли внизу живота.
- Осложнения со стороны желудочно-кишечного тракта. У больных могут возникать острые эрозии и язвы желудочно-кишечного тракта. Причина их развития — выброс в кровь высоких доз глюкокортикоидных гормонов как ответ на стресс, что усиливает выделение желудочного сока. При застойной сердечной недостаточности развиваются отёк слизистых и гипоксия (недостаточное насыщение кислородом), вызывающие изменения слизистой оболочки желудочно-кишечного тракта. Острые эрозии и язвы желудка и двенадцатиперстной кишки проявляются болями после еды, возможны ночные и «голодные» боли, изжога, рвота. У лиц пожилого возраста частым осложнением инфаркта становится парез (непроходимость) желудочно-кишечного тракта из-за уменьшения тонуса кишечной стенки и паралича мускулатуры кишечника. Основные симптомы — икота, ощущение переполненности желудка после еды, рвота, выраженное вздутие живота, отсутствие стула, разлитая болезненность живота при ощупывании.
- Постинфарктный аутоиммунный синдром Дресслера. Развивается у 3-4 % больных со 2 по 8 неделю после начала инфаркта миокарда. Иммунная система при этом синдроме начинает атаковать собственные клетки, воспринимая здоровые ткани в качестве чужеродных элементов. Это проявляется в виде следующих симптомов: перикардит (воспаление перикарда), плеврит (воспаление плевры), пневмонит (воспаление в тканях лёгких), лихорадка, повышение в крови эозинофилов, увеличение СОЭ (скорости оседания эритроцитов). Часто в воспалительный процесс вовлекаются суставы, развивается синовит (воспаление в синовиальной оболочке сустава), чаще поражаются крупные плечевые, локтевые, лучезапястные суставы.
- Синдром передней грудной клетки. Синдром плеча и руки. Развиваются у больных с остеохондрозом межпозвонковых дисков шейно-грудного отдела позвоночника спустя несколько недель и даже месяцев после возникновения инфаркта миокарда. При синдроме передней стенки грудной клетки возникает поражение грудинно-рёберных суставов. Появляется припухлость и боль в окологрудинных областях, усиливающиеся при надавливании на грудину и грудинно-рёберные сочленения, при поднятии рук кверху. При синдроме плеча и руки возникают боли в левом плечевом суставе (чаще всего), также могут быть боли в правом или в обоих плечевых суставах. Боли усиливаются при движении.
- Психические нарушения. Нарушения психики обычно развиваются на первой неделе заболевания из-за нарушения гемодинамики мозга, гипоксемии (понижения содержания кислорода в крови) и влияния продуктов распада некротического (омертвевшего) очага миокарда на головной мозг. Чаще всего расстройства психики наблюдаются у больных старше 60-ти лет с атеросклерозом сосудов головного мозга. Возникают психотические (оглушённость, оцепенение, делирий, сумеречные состояния) и непсихотические реакции (депрессивный синдром, эйфория).
Диагностика инфаркта миокарда
Постановка диагноза в большинстве случаев не представляет трудностей. Врач опирается на типичную клиническую картину, данные электрокардиографии и определение в крови биомаркеров некроза сердечной мышцы.
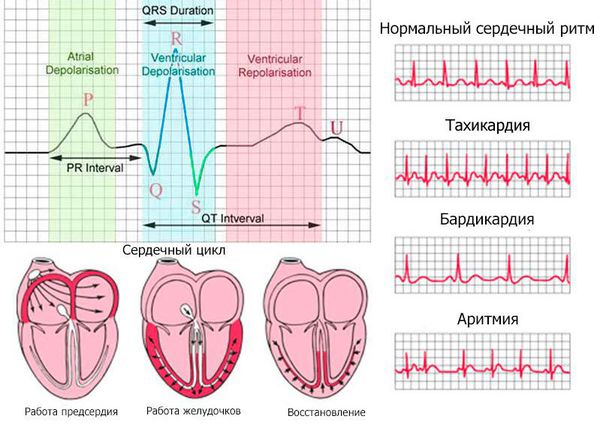
При подозрении на инфаркт миокарда сразу же необходимо выполнить ЭКГ (электрокардиография). Если есть возможность, рекомендуется сравнить ЭКГ, записанную в момент болевого приступа, с ранее зарегистрированной ЭКГ. ЭКГ следует записывать неоднократно, делая динамическое ЭКГ-наблюдение: иногда в первые часы и даже несколько первых дней ЭКГ-признаки инфаркта неубедительны, и только на последующих ЭКГ появляется характерная картина болезни. В стационаре наиболее целесообразно проводить ЭКГ-мониторирование в течение 24 часов от начала развития инфаркта миокарда.
Лабораторные исследования включают в себя:
- Общий анализ крови. Отражает резорбционно-некротический синдром. Начиная с 4-6-го часа инфаркта миокарда на фоне нормальных значений СОЭ начинает появляться лейкоцитоз (повышение числа лейкоцитов) нередко со сдвигом формулы влево. Лейкоцитоз сохраняется до четырёх дней и к концу первой недели снижается. Начиная со второго дня инфаркта миокарда постепенно начинает расти СОЭ. К началу второй недели заболевания число лейкоцитов нормализуется. Сохранение лейкоцитоза и/или умеренной лихорадки более недели свидетельствует о возможном наличии осложнений: плеврита, пневмонии, перикардита, тромбоэмболии мелких ветвей лёгочной артерии и др.
- Биохимический анализ сыворотки крови. Маркерами гибели клеток сердечной мышцы (миоцитов) являются изменения концентрации в крови креатинфосфокиназы (КФК), лактатдегидрогеназы (ЛДГ), аспартатаминотрансферазы (АСАТ), а также содержание в крови миоглобина, кардиотропонинов Т и I (TnI и TnT) [2] .
Эхокардиография позволяет выявить такие осложнения острого инфаркта миокарда, как образование пристеночных тромбов в полостях сердца, появление аневризмы сердца, разрыв межжелудочковой перегородки или отрыв сосочковых мышц. С помощью эхокардиографии выявляется важнейший признак инфаркта миокарда — нарушения локальной сократимости миокарда. Эти нарушения соответствуют распространённости некроза.
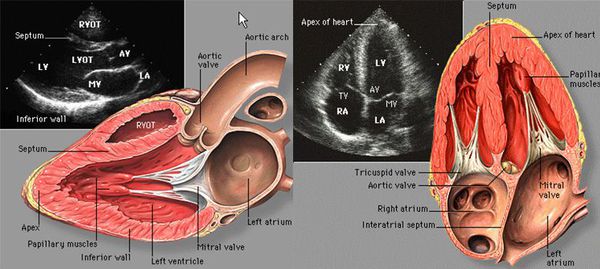
Экстренная селективная коронарная ангиография проводится в тех случаях, когда ЭКГ и анализ активности ферментов не дают результатов, либо же их интерпретация затруднена (например, в условиях наличия сопутствующих заболеваний, «смазывающих» картину). Исследование представляет собой рентгеновский снимок сосудов сердца, в которые предварительно введено контрастное вещество. С помощью ангиографии (коронарографии) можно установить закупорку коронарной артерии тромбом и снижение сократимости желудочка. С помощью этого метода оценивают, можно ли провести аортокоронарное шунтирование или ангиопластику — операции, восстанавливающие кровоток в сердце [7] .
Лечение инфаркта миокарда
Пациента с острым инфарктом необходимо оперативно доставить в стационар для профилактики осложнений и повышения шансов на выживание. Система оказания помощи больным инфарктом миокарда включает следующие этапы:
- Догоспитальный этап. Помощь оказывают бригады скорой помощи, они же транспортируют больного в стационар.
- Госпитальный этап. Помощь оказывается в специализированных сосудистых отделениях.
- Реабилитационный этап. Реабилитация проводится в специальных отделениях больниц или специализированных кардиологических санаториях.
- Диспансерное наблюдение и амбулаторное лечение. Диспансеризация в постинфарктном периоде осуществляется в областных или городских кардиологических центрах или в кардиологических кабинетах поликлиник [6] .
На догоспитальном этапе решаются следующие задачи:
- устанавливается точный диагноз. Если это не удаётся, допустимо установление ориентировочного синдромного диагноза в максимально короткое время;
- под язык больному дают таблетку нитроглицерина (или использовать нитросодержащий спрей) и 0,25-0,35 г аспирина;
- боль снимается введением обезболивающих;
- ликвидируется острая недостаточность кровообращения и нарушения ритма сердца;
- больного выводят из состояния кардиогенного шока;
- при клинической смерти производят реанимационные мероприятия;
- как можно скорее транспортируют больного в стационар.
Дальнейшая терапия определяется стадией (периодом) инфаркта миокарда. В остром и острейшем периоде цель лечения — предотвращение увеличения очага омертвения миокарда, устранение боли и других симптомов. Важно восстановить ток крови по сердечным артериям и купировать боль. Интенсивность боли в этом периоде настолько велика, что пациент может погибнуть из-за остановки сердца. Необходимо провести профилактику тяжёлых осложнений. При переходе болезни в подострую стадию и в постинфарктном периоде цель терапии — снижение риска рецидива приступа и возможных осложнений.
Для лечения острого инфаркта миокарда используются лекарственные препараты из различных фармакологических групп:
Обезболивающие препараты. Анальгетики из группы наркотических обезболивающих (морфин, промедол, омнопон) в сочетании с анальгином, антигистаминными препаратами (димедрол). Наиболее эффективной является нейролептанальгезия, когда используется комбинация анальгетика фентанила с сильным нейролептиком дроперидолом. Эффективность применения этих препаратов заметна уже через несколько минут. Исчезает не только боль, но и страх смерти, немотивированная тревога и психомоторное возбуждение. Для снятия психомоторного возбуждения могут использоваться транквилизаторы (диазепам). Для уменьшения гипоксии (снижения кислорода в тканях) используются ингаляции кислорода с помощью носового катетера.
Тромболитическая терапия. Важно восстановить ток крови и растворить тромбы, чтобы омертвение сердечной мышцы на распространялось дальше. Чем меньше зона некроза, тем выше шансы больного на успешную реабилитацию и ниже риск опасных для жизни осложнений. Немедленное применение препаратов (желательно в течение первого часа после приступа) позволяет достичь максимальную эффективность лечения. Допускается временной лимит в пределах трёх часов. Для растворения тромба внутривенно вводятся тромболитические препараты, например, стрептокиназа, урокиназа, альтеплаза. Доза зависит от веса пациента.
Восстановление коронарного кровотока возможно также с помощью хирургического лечения — стентирования или аорто-коронарного шунтирования. Баллонный катетер вводится в узкий участок артерии под контролем рентгеноскопии. При этом атеросклеротическая бляшка «раздавливается», а просвет артерии сердца увеличивается. Затем в просвет сосуда может быть установлен стент (металлический каркас).
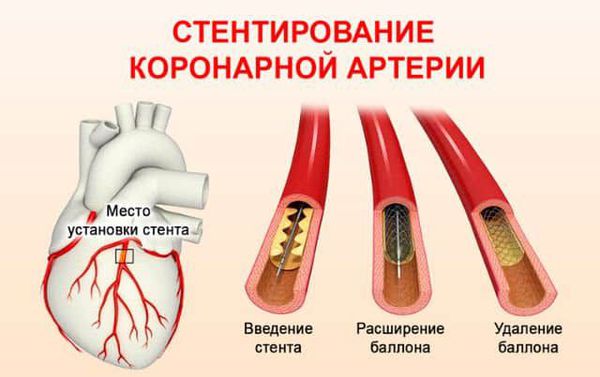
Антиагреганты. Препараты из этой группы влияют на клетки крови (тромбоциты и эритроциты). Действие антиагрегантов препятствует слипанию тромбоцитов, улучшая кровоток. Основным применяемыем препаратом является аспирин (ацетилсалициловая кислота). Противопоказания к применению аспирина: кровотечения из желудочно-кишечного тракта, обострение язвы желудка или двенадцатиперстной кишки.
Используются также ингибиторы P2Y12-рецепторов тромбоцитов, которые блокируют активацию тромбоцитов. Основные блокаторы — тикагрелор, прасугрел и клопидогрел.
Внутривенные/подкожные антикоагулянты. При остром коронарном синдроме для профилактики тромбоза глубоких вен (ТГВ) и тромбоэмболии легочной артерии (ТЭЛА) в остром периоде применяется нефракционированный гепарин (НФГ), который вводится внутривенно. Эноксапарин, который используется также для профилактики венозных тромбоэмболий, вводится подкожно.
Чтобы ограничить зону ишемии и некроза миокарда необходимо кроме восстановления кровотока в артериях сердца уменьшить гемодинамическую нагрузку на сердце. С этой целью используются нитраты и бета-блокаторы.
Нитраты. Оказывают противоболевой эффект, уменьшают потребность миокарда в кислороде, увеличивают коронарный и коллатеральный (обходной) кровоток, снижают нагрузку на сердечную мышцу, ограничивают размеры очага поражения миокарда. Особенно эффективна комбинация их с бета-блокаторами, приводящая к быстрой положительной динамике ЭКГ и снижению риска внезапной смерти [10] .
Бета-адреноблокаторы оказывают антиаритмическое действие. Цель применения бета-адреноблокаторов (пропранолола, метопролола, атенолола) — уменьшение частоты и силы сердечных сокращений, что поможет уменьшить нагрузку на сердце и потребность миокарда в кислороде. Бета-блокаторы продолжают применять при отсутствии побочных эффектов и противопоказаний неопределённо длительное время [1] .
Прогноз. Профилактика
Общий уровень смертности от инфаркта миокарда составляет примерно 30 %, от 50 до 60 % больных умирают на догоспитальном этапе. Летальность в стационаре составляет около 10 %.
Клинические характеристики, предсказывающие высокую (до 90 %) смертность у больных:
- пожилой и старческий возраст (31 % общей смертности);
- низкое систолическое артериальное давление (24 %);
- высокая частота сердечных сокращений (12 %);
- передняя локализация инфаркта миокарда (6 %).
Смертность среди больных сахарным диабетом и женщин несколько выше.
Смертность среди пациентов с первичным инфарктом миокарда составляет 8-10 % в первый год после острого инфаркта миокарда. Большинство смертей происходит в первые 3-4 месяца. Постоянная желудочковая аритмия, сердечная недостаточность и сохраняющаяся ишемия являются маркерами высокого риска смерти. Низкая переносимость физических нагрузок также ассоциируется с плохим прогнозом.
Профилактика инфаркта миокарда подразделяется на первичную и вторичную [3] .
Первичная профилактика проводится при наличии каких-либо проблем с сердцем, но до того, как произошёл инфаркт. В неё входят:
- Физическая активность — малоподвижный образ жизни отрицательно влияет на сердечно-сосудистую систему, а занятия спортом помогают сбросить избыточный вес, повышающий риск атеросклероза и нагрузку на сердце.
- Отказ от вредных привычек — курение табака способствует развитию и прогрессированию атеросклероза. Алкоголь следует употреблять в небольшом количестве. Излишнее употребление алкоголя оказывает токсическое действие на сердечную мышцу и другие органы, может вызывать аритмии и сосудистый спазм (сужение сосудов).
- Правильное питание — включение в ежедневный рацион свежих овощей, фруктов и зелени. Жирное мясо (свинину) лучше заменить на мясо птицы или кролика. Полезны рыба и морепродукты. Необходимо ограничить приём соли. При экстрасистолии нельзя употреблять пряности, так как они могут спровоцировать развитие аритмии.
- Контроль над стрессом — отдых, полноценный сон (не менее восьми часов в сутки). Стрессы и депрессии могут провоцировать инфаркт, так как под их влиянием происходит спазм сосудов сердца. Некоторым людям необходимо пройти курс лечения у психолога.
- Регулярные посещения кардиолога — после 40 лет осмотр рекомендуется делать ежегодно. Обязательно необходимо делать ЭКГ-исследование, проводить определение липидного профиля (общего холестерина и его фракций), контролировать уровень сахара в крови.
- Контроль за давлением — разрыв атеросклеротической бляшки зачастую провоцирует повышенное артериальное давление. При выявленной артериальной гипертензии необходим своевременный постоянный приём гипотензивных (снижающих артериальное давление) препаратов, назначенных кардиологом.

Вторичная профилактика инфаркта миокарда необходима тем, кто уже перенёс инфаркт. Она направлена на предотвращение повторного инфаркта миокарда и длится всю жизнь. Помимо мер, которые применяются для первичной профилактики инфаркта, обязательно постоянное применение медикаментозных препаратов, назначенных врачом:
- двойная антиагрегантная терапия (аспирин и второй антиагрегант — тикагрелор или клопидогрел) в течение года после инфаркта миокарда для снижения риска сердечно-сосудистых событий; п ервичная профилактика аспирином не нужна;
- бета-блокаторы для уменьшения частоты сердечных сокращений и снижения уровня артериального давления;
- статины для снижения уровня холестерина и предотвращения прогрессирования атеросклероза;
- нитраты для купирования болевых приступов при возобновлении стенокардии;
- ингибиторы АПФ или сартаны для нормализации артериального давления, а также при наличии признаков сердечной недостаточности.
Обязателен регулярный контроль за состоянием больного, уровнем артериального давления, показателями биохимии (в частности уровнем печёночных ферментов и показателями липидного профиля), изменениями на ЭКГ, эхокардиографии. При необходимости проводится суточное мониторирование ЭКГ.
Список литературы
- Гиляревский С. Р. Роль противоишемических препаратов в эпоху реваскуляризации миокарда. — М., 2010. — С. 29.
- Внутренние болезни: Учебник / Под ред. А. И. Мартынова, Н. А. Мухина, В. С. Моисеева, А. С. Галявича. — М.: ГЭОТАР-МЕД, 2004. — Т. 1. — 600 с.
- Кардиоваскулярная профилактика: Национальные рекомендации. — М., 2011. — 96 с.
- Кук-Суп Со Клиническая интерпретация ЭКГ. Введение в электрокардиографию. — М.: МЕДпресс-информ, 2015. — С. 98-124.
- Окороков А. Н. Диагностика болезней внутренних органов: Т 6. Диагностика болезней сердца и сосудов. — М.: Мед.лит., 2002. — С. 449.
- Окороков А. Н. Лечение болезней внутренних органов: Т 3. Лечение болезней сердца и сосудов. — М.: Мед.лит., 2000. — С. 464.
- Суворов А. В. Клиническая электрокардиография. — Нижний Новгород: Изд-во НМИ, 1993. — С. 67-81.
- Фомина И. Г. Нарушения сердечного ритма. — М.: Издательский дом «Русский врач», 2003. — 192 с.
- Alter D. A. Socioeconomic status and mortality after acute myocardial infarction // Ann. Intern. Med. — 2006; 144 (2): 55-61.ссылка
- Росстат. Демографический ежегодник России. — М., 2014.
- Kanamsa K., Natio N., Morii H., et al. Eccentric dosing of nitrates does not increase cardiac events in patients with healed myocardial infarction // Hypertens Res. — 2004; 27: 563-572.ссылка
Источник https://diseases.medelement.com/disease/%D0%BE%D1%81%D1%82%D1%80%D1%8B%D0%B9-%D0%B8%D0%BD%D1%84%D0%B0%D1%80%D0%BA%D1%82-%D0%BC%D0%B8%D0%BE%D0%BA%D0%B0%D1%80%D0%B4%D0%B0-%D0%BD%D0%B5%D1%83%D1%82%D0%BE%D1%87%D0%BD%D0%B5%D0%BD%D0%BD%D1%8B%D0%B9-i21-9/12338
Источник https://probolezny.ru/infarkt-miokarda/