Ревматоидный артрит
Научный редактор: Строкина О.А., терапевт, врач функциональной диагностики.
Ноябрь, 2019.
Ревматоидный артрит — воспалительное заболевание, характеризующееся симметричным поражением суставов и воспалением внутренних органов.
Распространенность и причины
На 2018 год в России зафиксировано около 300 тыс. пациентов с ревматоидным артритом (~0,61% взрослого населения). В целом по миру процент больных колеблется от 0,5 до 2%.
Женщины страдают в 3 раза чаще мужчин. Пик заболеваемости ревматоидным артритом — 40-55 лет, но встречается и в более молодом возрасте. Половина пациентов в первые 3-5 лет заболевания теряет трудоспособность.
Причина возникновения ревматоидного артрита неизвестна. В последнее время исследователи склоняются к тому, что ведущая причина развития ревматоидного артрита — сочетание внутренних факторов (генетика, выработка половых гормонов) и факторов окружающей среды (бактериальные и вирусные инфекции, профессиональные вредности, стрессы).
Доказано, что табакокурение является ведущим внешним фактором в развитии патологии. Опубликованы результаты масштабного исследования, говорящие о том, что пассивное курение в детском возрасте также значительно увеличивает риск развития ревматоидного артрита во взрослом возрасте 1 .
Симптомы ревматоидного артрита
Развитие заболевания происходит постепенно. Сначала появляются общие симптомы и слабо выраженные симптомы поражения суставов.
Общие признаки
- Быстрая утомляемость — как правило, появляется за несколько недель или месяцев до развития других симптомов. Усталость может быть как постоянной, так и периодической.
- Небольшое повышение температуры тела в сочетании с суставными симптомами (при этом температура выше 38С обычно не характерна для ревматоидного артрита).
- Проблемы с глазами (зуд, воспаление или выделения) — Синдром Шегрена.
- Похудение.
Ревматоидные узелки – плотные подкожные образования, в типичных случаях локализованные в областях, часто подвергающихся травматизации (например, в области локтевого отростка, на разгибательной поверхности предплечья). Наблюдаются у 20-50 % пациентов. Очень редко обнаруживают во внутренних органах (например, в легких).
В некоторых случаях наблюдается увеличение селезенки.
Также при ревматоидном артрите могут проявляться признаки остеопороза (это разрежение костной ткани), амилоидоза.
Нередкими бывают язвы на коже голеней, воспаления артерий.
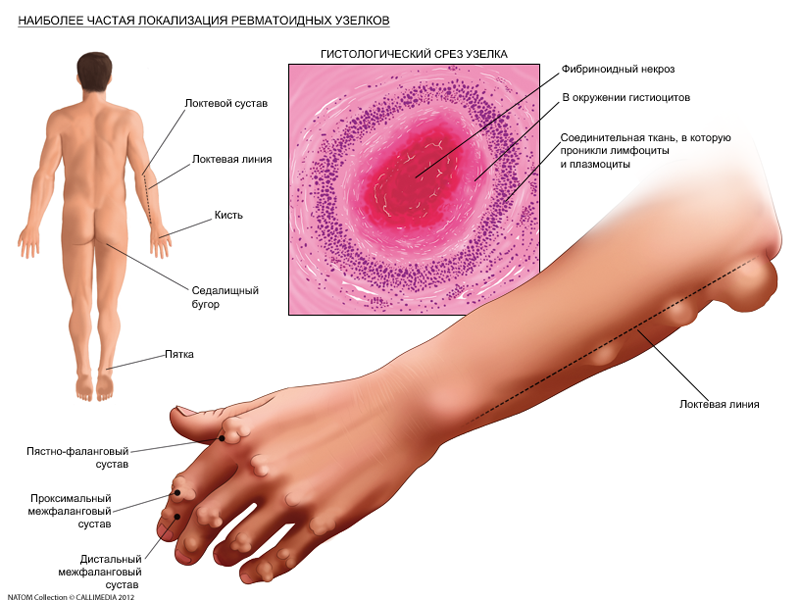
Фото: локализация ревматоидных узелков
Поражение суставов
Симметричность поражения суставов – важная особенность ревматоидного артрита (например, поражаются правый и левый локтевые суставы или правый и левый коленные суставы)
- Утренняя скованность суставов длительностью более 1 часа — один из ранних признаков ревматоидного артрита.
- По мере прогрессирования, скованность появляется при любом длительном бездействии, время которого постепенно сокращается. Обычно начинается с суставов пальцев и запястий.
- Увеличение пораженных суставов в размерах.
- Онемение и покалывание в руках — воспалившиеся сухожилия могут сдавливать нервы 2 .
Усталость является одним из «изнуряющих» симптомов ревматоидного артрита (как и для многих других аутоиммунных заболеваний). Проблема борьбы с усталостью и быстрой утомляемостью при аутоиммунных заболеваниях в последнее время получает все более пристальное внимание, по данным исследования 2018 года, именно патологическая усталость является одной из причин снижения работоспособности у людей с ревматоидным артритом 3 .
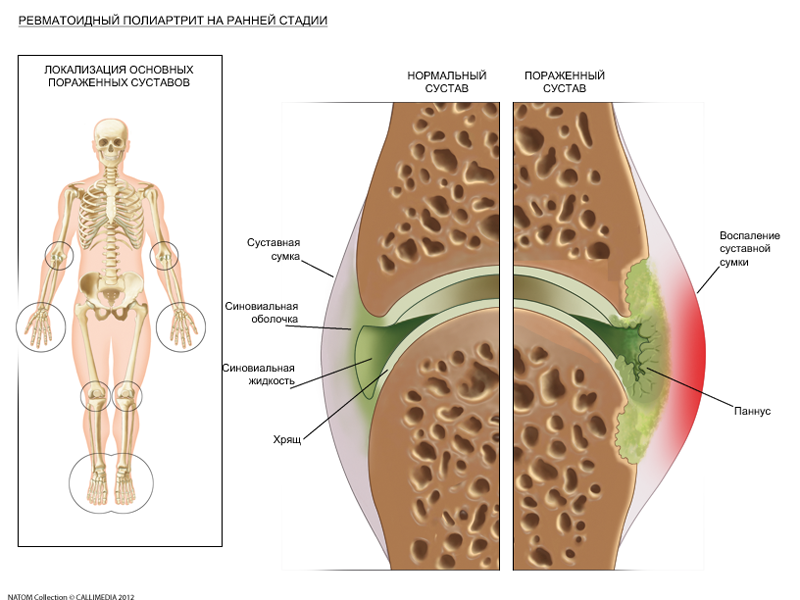
Фото: суставы-мишени и механизм поражения сустава при ревматоидном артрите ранней стадии.
Неспецифические показатели крови
- Анемия вследствие замедления обмена железа в организме, вызванного нарушением функций печени;
- Снижение количества тромбоцитов, нейтрофилов.
Распространенные схемы начала заболевания
Ревматоидный артрит может начинаться по-разному. Ниже описаны наиболее распространенные суставные симптомы, характерные для начала заболевания:
- Боль и скованность нарастают постепенно, чаще в мелких суставах кистей. Обычно проявления не связаны со временем суток. Обязательно поражаются симметричные суставы. Длительность нарастания симптомов — несколько месяцев.
- Явно выраженная скованность суставов кистей и стоп по утрам. В этом случае характерно раннее выявление ревматоидного фактора в крови.
- Рецидивирующий теносиновит, особенно часто в области лучезапястных суставов (воспаление сухожилия, характеризуется припухлостью, болью и отчетливым скрипом во время движения).
- Воспаление коленных или плечевых суставов с последующим быстрым вовлечением в процесс мелких суставов кистей и стоп.
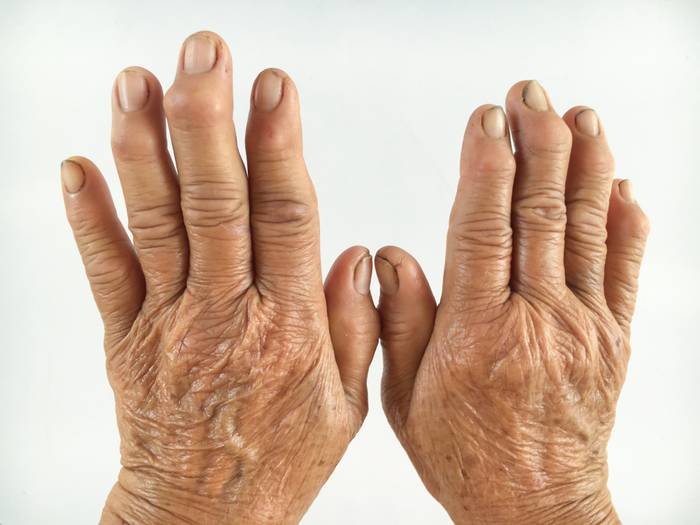
Также стоит иметь ввиду, что у значительной части больных ревматоидный артрит начинается с нехарактерных проявлений, например, с воспаления крупных, а не мелких суставов.
Фото: деформированные суставы при ревматоидном артрите
Диагностика
Важные признаки
Критерии диагноза ревматоидного артрита Американской ревматологической ассоциации. Наличие по крайней мере 4 из следующих признаков:
- утренняя скованность более 1 часа;
- артрит 3 и более суставов;
- артрит суставов кистей;
- симметричный артрит;
- ревматоидные узелки;
- положительный ревматоидный фактор;
- рентгенологические изменения.
Лабораторные исследования
В общем и биохимическом анализе крови:
- анемия,
- увеличение СОЭ,
- повышение содержания С-реактивного белка.
Ревматоидный фактор (антитела к иммуноглобулинам класса M) положителен в 70-90% случаев.
Высокие значения АЦЦП (антитела к циклическому цитруллинированному пептиду).
Суставная жидкость мутная, с низкой вязкостью, повышено количество лейкоцитов и нейтрофилов.
Инструментальные исследования
Минздрав РФ рекомендует всем пациенам с подозрением на ревматоидный артрит проходить обзорную рентгенографию кистей и стоп. Это позволяет верифицировать заболевание и определить его стадию, при наличии.
При неоднозначных результатах рентгенографии может врач может назначить МРТ суставов, т.к. МРТ — более чувствительный метод.
По показаниям может быть назначено УЗИ мелких суставов или рентгенография крупных. При подозрении на поражение легких назначается КТ.
Лечение ревматоидного артрита
Лекарственная терапия включает применение трех групп препаратов:
- базовые препараты
- нестероидные противовоспалительные (НПВП)
- глюкокортикоиды
Базисные препараты
Базисные препараты рекомендуется применять сразу после установления диагноза.
Основными лекарственными средствами базисной терапии ревматоидного артрита являются:
- Метотрексат
- Лефлуномид
- Сульфасалазин
- Гидроксихлорохин
В России 4 стандартом лечения является терапия метотрексатом или его комбинацией с сульфасалазином и гидроксихлорохином. Базовые препараты необходимо начинать как можно раньше.
Неэффективные на протяжении 1,5-3 месяцев базисные препараты должны быть заменены или использованы их комбинации с гормонами в малых дозах, что позволяет снизить активность ревматоидного артрита.
Шесть месяцев – критический срок от начала симптомов поражения суставов, не позднее которого должна быть подобрана действенная базисная терапия.
В процессе лечения базисными препаратами тщательно мониторируют активность болезни и побочные эффекты. Необходимо контролировать показатели общего анализа крови, АСТ, АЛТ и креатинин.
Важно! На фоне лечения метотрексатом для уменьшения риска развития нежелательных реакций рекомендуется принимать фолиевую кислоту, не менее 5 мг в неделю. Ее принимают по прошествии суток после прима метотрексата.
Нестероидные противовоспалительные препараты
Чаще других применяются следующие НПВС:
- диклофенак,
- нимесулид,
- мелоксикам,
- кетопрофен,
- целекоксиб.
Эти препараты имеют минимальный побочный эффект и сохраняют высокую противовоспалительную и обезболивающую активность.
Мелоксикам (мовалис) в начале лечения при активности воспалительного процесса назначают по 15 мг/сут., а в дальнейшем переходят на 7,5 мг/сут. в качестве поддерживающей терапии.
Нимесулид назначается в дозе 100 мг два раза в сутки.
Целекоксиб (целебрекс) назначается по 100-200 мг два раза в сутки.
Для пожилых людей подбор дозировки препарата не требуется. Однако у пациентов с массой тела ниже средней (50 кг) желательно начинать лечение с самой низкой рекомендованной дозы.
Следует избегать комбинации двух или более нестероидных противовоспалительных препаратов, поскольку их эффективность остается неизменной, а риск развития побочных эффектов возрастает.
Глюкокортикостероиды (гормоны)
При высокой степени активности воспаления используют гормоны, причем в случаях системных проявлений ревматоидного артрита – в виде пульс-терапии (только гормоны или в сочетании с цитостатиком – циклофосфамидом), без системных проявлений – в виде курсового лечения. Обычно применяют преднизолон.
Гормоны также применяют как поддерживающую противовоспалительную терапию при неэффективности других лекарственных средств.
В ряде случаев гормоны используются в качестве местной терапии.
Мази, кремы, гели на основе нестероидных противовоспалительных препаратов (ибупрофен, пироксикам, кетопрофен, диклофенак) используют в виде аппликаций на воспаленные суставы.
Для усиления противовоспалительного эффекта аппликации вышеназванных мазевых форм препаратов сочетают с аппликациями раствора диметилсульфоксида в разведении 1:2-1:4.
Дополнительная терапия
При отсутствии ответа на стандартное лекарственное лечение у больных с высокой активностью ревматоидного артрита применяют плазмаферез, лимфоцитаферез.
Важным моментом в лечении ревматоидного артрита является профилактика остеопороза – восстановление нарушенного кальциевого баланса в направлении повышения всасывания его в кишечнике и уменьшения выведения из организма.
Для этого применяется диета с повышенным содержанием кальция.
Источниками кальция являются молочные продукты (особенно твердые сорта сыра, а также плавленый сыр; в меньшей степени творог, молоко, сметана), миндаль, лесные и грецкие орехи и пр., а также препараты кальция в сочетании с витамином D или его активными метаболитами.
Препаратом, который можно отнести к базисным антиостеопоретическим средствам, является миакальцик. Он выпускается для внутримышечного введения по 100 ME и в виде назального спрея; назначается по схеме совместно с препаратами кальция (кальцитонин) и производными витамина D.
При лечении ревматоидного артрита используется также лазерная терапия. Особенно при тяжелых обострениях ревматоидного артрита в последние годы широко используются внекорпоральные методы лечения (в первую очередь гемосорбция и плазмаферез).
Лазеротерапия особенно показана на ранней стадии процесса. Курс не более 15 процедур.
С целью уменьшения боли и устранения спазма околосуставных тканей применяется криотерапия (лечение холодом), на курс 10–20 процедур.
С целью воздействия на аллергические процессы, улучшения питания тканей и устранения воспаления применяют и другие физические методы лечения.
В ранней стадии ревматоидного артрита рекомендуется ультрафиолетовое облучение пораженных суставов, электрофорез диметилсульфоксида, кальция, салицилатов.
При появлении более стойких изменений в суставах и при отсутствии признаков высокой активности назначают фонофорез гидрокортизона, магнитотерапию, импульсные токи.
Лечебная физкультура и массаж назначаются всем больным с целью снятия мышечного спазма, быстрейшего восстановления функции суставов.
Все больные ревматоидным артритом должны систематически наблюдаться и обследоваться ревматологом.
Больные с медленно прогрессирующим течением без поражения внутренних органов должны появляться у ревматолога 1 раз в 3 месяца. При наличии поражения внутренних органов больные осматриваются ревматологом 1 раз в 2-4 недели.
Курортное лечение больных ревматоидным артритом рекомендуется осуществлять ежегодно вне фазы обострения.
При доброкачественном течении процесса без выраженных изменений суставов показано применение радиоактивных ванн в Цхалтубо и Белокурихе; при типичном прогрессирующем процессе – лечение сероводородными ваннами в Сочи, Серноводске, Пятигорске, Кемери; при выраженных деформациях и контрактурах – лечение грязевыми аппликациями в Евпатории, Саках, Пятигорске, Одессе.
- 1.Пассивное курение провоцирует ревматоидный артрит. — Performance media, 2017.
- 2. Brenda B. Spriggs, MD, MPH. Early Signs of Rheumatoid Arthritis. — Healthline, Sep 2018.
- 3. Ashley Boynes Shuck. What People with Rheumatoid Arthritis Can Do About the ‘Unrelenting’ Effects of Fatigue. — Healthline, Oct 2019.
- 4.Ревматоидный артрит. Клинические рекомендации. — Министерство Здравоохранения РФ, 2018.
(c) Diagnos.ru, 2002-2021. Контакты: .
Важно! Все материалы носят справочный характер и ни в коей мере не являются альтернативой очной консультации специалиста.
Этот сайт использует cookie-файлы для идентификации посетителей сайта: Google analytics, Yandex metrika, Google Adsense. Если для вас это неприемлемо, пожалуйста, откройте эту страницу в анонимном режиме.
Ревматоидный артрит поздняя стадия лечение
7 августа 2023 Регистрация Войти
7 сентября 2023
(1).jpg)
Об актуальных изменениях в КС узнаете, став участником программы, разработанной совместно с АО »СБЕР А». Слушателям, успешно освоившим программу, выдаются удостоверения установленного образца.
15 августа 2023
Программа разработана совместно с АО »СБЕР А». Слушателям, успешно освоившим программу, выдаются удостоверения установленного образца.
Продукты и услуги Информационно-правовое обеспечение ПРАЙМ Документы ленты ПРАЙМ Клинические рекомендации «Ревматоидный артрит» (утв. Министерством здравоохранения РФ, 2021 г.)

Обзор документа
Клинические рекомендации «Ревматоидный артрит» (утв. Министерством здравоохранения РФ, 2021 г.)
18 октября 2021
МКБ 10: М05, М0 6
Возрастная категория: взрослые
Год утверждения: 2021
— Ассоциация ревматологов России
— ОООИ «Российская ревматологическая ассоциация «Надежда»
Список сокращений
АЛА — анти-лекарственные антитела
АЦБ — антитела к циклическим цитруллинированным белкам
АЦЦП — антитела к циклическому цитруллинированному пептиду
сБПВП — синтетические базисные противовоспалительные препараты
ВАШ — визуально-аналоговая шкала
ВГН — верхняя граница нормы
ВИЧ — вирус иммунодефицита человека
ВП — внесуставные проявления
ГИБП — генно-инженерные биологические препараты
ИБС — ишемическая болезнь сердца
ИЗЛ — интерстициальное заболевание легких
— ингибиторы фактора некроза опухоли альфа (ФНО-альфа)
IgG — иммуноглобулин G
ЛПВП — липопротеины высокой плотности
ЛПНП — липопротеины низкой плотности
ЛФК — лечебная физкультура
ММП — матриксные металлопротеиназы
МПС — макрофагоподобные синовиоциты
МРТ — магнитно-резонансная томография
НЛР — нежелательные лекарственные реакции
НПВП — нестероидные противовоспалительные препараты
ОБП — оценка боли пациентом
ООЗП — общая оценка заболевания пациентом
ПЛФС — плюснефаланговый сустав
ПМФС — проксимальный межфаланговый сустав
ПФС — пястнофаланговый сустав
РА — ревматоидный артрит
РКИ — рандомизированные клинические исследования
РФ — ревматоидный фактор
СИР — стандартные инфузионные реакции
СКВ — системная красная волчанка
СОЭ — скорость оседания эритроцитов
СРВ — С-реактивный белок
тсБПВП — таргетные синтетические БПВП
ФПС — фибробластополобные синовиоциты
УЗИ — ультразвуковое исследование
ЧБС — число болезненных суставов
ЧПС — число припухших суставов
ХСН — хроническая сердечная недостаточность
ЦЗТ — цертолизумаба пэгол**
ACR — American College of Rheumatology
CDAI — Clinical Disease Activity Index
DAS — Disease Activity Index
EULAR — European League Against Rheumatism
HAQ — Health Assessment Questionnaire
NICE — National Institute for Health and Care Excellence
SDAI — Simplified Disease Activity Index
Термины и определения
Недифференцированный артрит (НДА) — воспалительное поражение одного или нескольких суставов, которое не может быть отнесено к какой-либо определенной нозологической форме, поскольку не соответствует классификационным критериям ревматоидного артрита (РА) или какого-либо другого заболевания.
Ранний РА — длительность менее 12 месяцев (с момента появления симптомов болезни, а не постановки диагноза РА).
Развернутый РА — длительность более 12 месяцев, соответствующий классификационным критериям РА (ACR/EULAR, 2010 г.).
Клиническая ремиссия РА — отсутствие признаков активного воспаления, критерии ремиссии: — число болезненных суставов (ЧБС), число припухших суставов (ЧПС), С-реактивный белок (СРБ, мг/%) и общая оценка заболевания пациентом (ООЗП, по ВАШ) меньше или равно 1 или CDAI меньше или равно 2,8 (критерии ACR/EULAR, 2011 г.).
Стойкая ремиссия РА — клиническая ремиссия длительностью 6 месяцев и более.
Противоревматические препараты — противовоспалительные препараты с различной структурой, фармакологическими характеристиками и механизмами действия, использующиеся для лечения РА и других ревматических заболеваний.
Нестероидные противовоспалительные препараты (НПВП) — группа синтетических лекарственных средств, обладающих симптоматическим обезболивающим, жаропонижающим и противовоспалительным эффектами, связанными в первую очередь с ингибицией активности циклооксигеназы — фермента, регулирующего синтез простагландинов.
Глюкокортикоиды (ГК) — синтетические стероидные гормоны, обладающие естественной противовоспалительной активностью.
Низкие дозы ГК — Низкие дозы ГК — менее 7,5 мг/день преднизолона (или эквивалентная доза другого ГК).
Средние дозы ГК — 7.5-30 мг/день преднизолона (или эквивалентная доза другого ГК).
Высокие дозы ГК — более 30 мг/день преднизолона (или эквивалентная доза другого ГК).
Синтетические базисные противовоспалительные препараты (сБПВП) — группа синтетических противовоспалительных лекарственных препаратов химического происхождения, подавляющих воспаление и прогрессирование деструкции суставов.
Генно-инженерные биологические препараты (ГИБП) — группа лекарственных средств биологического происхождения, в том числе моноклональные антитела (химерные, гуманизированные, полностью человеческие) и рекомбинантные белки (обычно включают Fc-фрагмент IgG человека), полученные с помощью методов генной инженерии, специфически подавляющие иммуновоспалительный процесс и замедляющие прогрессирование деструкции суставов.
Ревматоидные факторы (РФ) — аутоантитела IgM, реже IgA и IgG изотипов, реагирующие с Fc-фрагментом IgG.
Антитела к цитруллинированным белкам (АЦБ) — аутоантитела, которые распознают антигенные детерминанты аминокислоты цитруллина, образующейся в процессе посттрансляционной модификации белков, наиболее часто определяются антитела к циклическому цитруллинированному пептиду (АЦЦП) и антитела к модифицированному цитруллинированному виментину (АМЦВ).
Нежелательная лекарственная реакция (HЛP) — любое неблагоприятное явление, которое развивается в момент клинического использования лекарственного препарата и не относится к его заведомо ожидаемым терапевтическим эффектам.
Липидный профиль — биохимический анализ, позволяющий объективизировать нарушения в жировом обмене организма, к которому относятся холестерин (ХС), липопротеиды высокой плотности (ЛПВП), липопротеиды низкой плотности (ЛПНП), триглицериды (ТГ).
Стандартные инфузионные реакции (СИР) — НЛР, связанные с проведением инфузии лекарственного препарата.
Таргетные синтетические БПВП (тсБПВП) — группа синтетических противовоспалительных лекарственных средств химического происхождения, по механизму действия специфически блокирующих функционирование внутриклеточных сигнальных путей «провоспалительных» и иммунорегуляторных цитокинов.
1. Краткая информация по заболеванию или состоянию (группе заболеваний или состояний)
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
Ревматоидный артрит (РА) — иммуновоспалительное (аутоиммунное) ревматическое заболевание, характеризующееся прогрессирующей деструкцией суставов и поражением внутренних органов, развитие которого определяется сложным взаимодействием факторов внешней среды и генетической предрасположенности, ведущих к глобальным нарушениям в системе гуморального и клеточного иммунитета [1, 2]. Гетерогенность патогенетических механизмов РА находит свое отражение в существовании широкого спектра фенотипов и эндотипов заболевания, что позволяет рассматривать его не как «одну болезнь», а как клинико-иммунологический синдром [3, 4].
При отсутствии эффективной терапии продолжительность жизни у больных РА ниже на 3 года у женщин и на 7 лет у мужчин, в первую очередь за счет высокого риска развития коморбидных заболеваний — кардиоваскулярной патологии, остеопороза, тяжелых инфекций, интерстициального заболевания легких, онкологических заболеваний [5]. У многих пациентов с РА жизненный прогноз столь же неблагоприятен, как и при лимфогранулематозе, сахарном диабете 2-го типа, трехсосудистом поражении коронарных артерий и инсульте. РА вызывает стойкую потерю нетрудоспособности у половины пациентов в течение первых 3-5 лет от начала болезни, а через 20 лет треть пациентов становятся полными инвалидами.
1.2 Этнология и патогенез заболевания или состояния (группы заболеваний или состояний)
Хотя этиология РА неизвестна, риск развития заболевания связан с широким спектром генетических, гормональных и внешнесредовых (курение, загрязнение воздуха, инфекционные агенты) и метаболических (дефицит витамина D, ожирение, низкое потребление полиненасыщенных жирных кислот) факторов, а также нарушениями микробиоты кишечника (ротовая полость, легкие). Патогенез РА определяется сложным взаимодействием факторов внешней среды и генетической предрасположенности, ведущих к глобальным нарушениям в системе врожденного и приобретенного иммунитета, которые выявляются задолго до развития клинических симптомов болезни [3, 6].
Суть патологического процесса при РА составляет системное аутоиммунное воспаление, которое с максимальной интенсивностью затрагивает синовиальную оболочку суставов. Эволюция РА включает несколько последовательно (или дискретно) развивающихся стадий: «преклиническая», которая трансформируются в «симптоматическую», завершающуюся формированием клинико-лабораторного симптомокомплекса, характерного для раннего, а затем развернутого РА. Предполагается, что развитие «субклинического» синовита наблюдается уже в «преклинической» стадии РА и связано с локальной микротравмой, повреждением микрососудов суставов, активацией системы комплемента и/или патогенным действием аутоантител (или иммунных комплексов), вызывающих активацию периартикулярных остеокластов, экспрессирующих цитруллинированные белки, которые вызывают деструкцию костной ткани, синтезом «провоспалительных» медиаторов, индуцирующих развитие боли и воспаления. В синовиальной ткани при РА выявляется массивная инфильтрация «иммунными» клетками (Т-лимфоциты, В-лимфоциты, плазматические клетки, макрофаги, тучные клетки, активированные стромальные клетки и синовиальные фибробласты), характер взаимодействия которых между собой и профиль синтеза «провоспалительных» медиаторов, существенно варьирует в зависимости от стадии болезни.
РА — классическое В-клеточное аутоиммунное заболевание, наиболее характерным проявлением которого является синтез широкого спектра аутоантител с различной специфичностью, которые обнаруживаются более, чем у 90% пациентов, страдающих РА. Кроме того, В-клетки участвуют в ко-стимуляции Т-клеток, вызывают активацию остеокластов (ОК) и синтезируют широкий спектр «провоспалительных» цитокинов — фактор некроза опухоли альфа , лимфотоксин, интерлейкин (ИЛ) 6 и др. Наиболее характерными для РА аутоантителами являются ревматоидные факторы (РФ) IgG, IgM и IgA изотипов, реагирующие с Fc-фрагментом молекулы IgG, и аутоантитела, реагирующие с антигенными эпитопами, универсальной характеристикой которых является пост-трансляционная модификация (цитруллинирование, карбамилирование, ацетилирование, перекисное окисление и др.). Основное значение придают цитруллинированию, которое представляет собой биохимический процесс, опосредованный ферментом петидил-аргинин дезаминазой (ПАД) 2 и 4, заключающийся в конверсии положительно заряженной аминокислоты аргинин в аминокислоту цитруллин, обладающую нейтральным зарядом. Гиперпродукция антител к цитрулинированным белкам (АЦБ) (особенно в комбинации с IgM и IgA РФ) ассоциируется с активностью заболевания, прогрессированием деструкции суставов, экстраартикулярными (системными) проявлениями, риском общей летальности, связанной с развитием коморбидных состояний, в первую очередь, кардиоваскулярных осложнений, «резистентностью» или напротив «чувствительностью» к фармакотерапии. Выделяют два основных клинико-иммунологических субтипа РА: АЦБ-позитивный и АЦБ-негативный. Они отличаются по молекулярным механизмам патогенеза, факторам генетической предрасположенности и внешней среды, тяжести течения и эффективности проводимой терапии. IgM РФ и АЦБ выявляются не только в сыворотках пациентов с РА, а также у пациентов с артралгией или неспецифическими мышечно-скелетными симптомами за много лет до развития РА, что рассматривается как важное доказательство существования «преклинической» системной «аутоиммунной» фазы этого заболевания. АЦБ (и РФ) являются не только чувствительными и специфичным биомаркерами РА, но могут иметь патогенетическое значение, выступая в роли дополнительных медиаторов воспаления и деструкции костной ткани. Это в свою очередь зависит от воздействия дополнительных экзогенных или эндогенных факторов (так называемый «второй сигнал» — second hit), усиливающих «провоспалительный» потенциал аутоантител. Развитие хронического воспаления суставов может быть связано с формированием так называемого «провоспалителыюго фенотипа» аутоантител, особенностями которого является нарушение гликозилирования (процесс присоединения моносахаридов к белку) Fc- и Fab-фрагментов молекулы иммуноглобулина.
Рассматривая механизмы, индуцирующие цитруллинирование, как потенциальный механизм формирования аутоантигенного репертуара, в первую очередь обращается внимание на курение, приводящее к избыточному образованию цитруллинированных белков в ткани легких. Наряду с тканью легких, важным местом образования ПТМ белков является ткань десен. Установлено увеличение распространенности РА у пациентов с периодонтитом, а также связь между развитием периодонтита, увеличением титров РФ и АЦБ и активностью РА. Полагают, что это связано со способностью Porphyromonas gingivalis (периодонтальный патоген) активировать ПАД, вызывающих цитруллинирование белков-мишеней для АЦБ (фибриноген, ). В последние годы большое значение в иммунопатогенезе РА придают дисбиозу микробиома, который, как полагают, может приводить к локальному воспалению, потере барьерной функции кишечника и траслокации кишечной бактериальной флоры в кровяное русло.
В генетических исследованиях системы HLA и при полногеномном поиске ассоциаций (genome-wide association studies — GWAS) выявлено более 100 однонуклеотидных полиморфизмов (single-nucleotide polymorphism — SNP), связанных с риском развития и прогрессирования РА. Особе значение имеет носительство антигенов II класса главного комплекса гистосовместимости — HLA-DR01/04, характерной особенностью которых является наличие общей аминокислотной последовательности (лейцин-глютамин-лизин-аргинин-аланин) в третьей гипервариабильной области цепей, которая получила название «общий эпитоп» (Shared Epitope — SE). Носительство HLA-DRB1*0401 выявляется у 50-61% пациентов с РА (ОР = 5-11), a HLA-DRB1*0404 — у 27-37% (ОР = 5-14). Молекулярной основой для этой ассоциации является тот факт, что положительный заряд этого участка молекулы HLA-DR блокирует связывание аргинин-содержащих пептидов, но облегчает (и усиливает аффинность) взаимодействие с цитруллинированными пептидами, нейтральный заряд. Доказана связь между носительством «общего эпитопа», факторами риска РА, индуцирующими цитруллинирование белков и гиперпродукцией РФ и АЦБ. Определенный вклад в предрасположенность к развитию РА вносят генетические полиморфизмы молекул, участвующих в ко-стимуляции Т-клеток (CD28, CD40, хемокины), гены рецепторов цитокинов (например, ИЛ6 и др.), ферментов, регулирующими пост-трансляционную модификацию белков, и гены различных белков — PTPN22 (Protein tyrosine phosphatase, non-receptor type 22), TNFAIP3 (Tumor necrosis factor, alpha-induced protein 3), STAT3 (signal transducer and activator of transcription 3), участвующих в иммунном ответе.
Развитие поражение суставов при РА, проявляющееся пролиферацией синовиальной ткани и деструкцией суставов, является сложным процессом в развитии которого принимают участие все элементы иммунной системы, включая Т и В лимфоциты, антиген-презентирующие клетки (В-клетки, макрофаги, дендритные клетки), которые синтезируют широкий спектр медиаторов воспаления и тканевой деструкции. Фундаментальный механизм развития РА связан с нарушением баланса между синтезом «провоспалительных» и «антивоспалительных» цитокинов, которые вызывают поляризацию иммунного ответа по Thelper (h) 1 и Th17 типам. Характерным морфологическим признаком РА является избыточный рост и пролиферация синовиальной ткани (панус), приводящей к образованию эрозий и деструкции костной ткани сустава. Внутренний (выстилающий) слой синовиальной ткани содержит 2 основных типа клеток: макрофагоподобные (тип А) и фибробластоподобные (тип В) синовиоциты. Макрофагоподобные синовиоциты (МПС) имеют гемопоэтическое, а фибробластоподобные синовиоциты (ФПС) — мезенхимальное происхождение. При РА синовиальная оболочка представляет собой гиперпластическую инвазивную ткань, формирование которой связано с усиленной миграцией этих клеток из костного мозга и кровотока, соответственно. МПС синтезируют широкий спектр «провоспалительных» медиаторов (цитокины, хемокины, факторы роста и др.), которые активируют ФПС, которые в свою очередь начинают активно синтезировать «провоспалительные» медиаторы и матриксные металлопротеиназы (ММП). Этот процесс способствует хронизации синовита и деструкции компонентов сустава. ФПС обладают выраженной способностью к инвазии, синтезу ММП и устойчивостью к апоптозу, связанному с гиперэкспрессией антиапоптотических белков. Хотя механизмы деструкции суставов чрезвычайно гетерогенны и связаны с синтезом «провоспалительных» медиаторов различными иммунными клетками (макрофаги, нейтрофилы, тучные клетки), доминирующую роль играют ФПС, экспрессирующие молекулу адгезии кадгерин-11, синтезирующие ММП, в первую очередь коллагеназу и стромелизин. Эрозия костной ткани опосредуется созреванием и активацией ОК, связанной с воздействием RANKL (receptor activator of nuclear factor-кВ), который синтезируется Т-клетками, а также , ИЛ-6 и ИЛ-1, синтезирующихся макрофагами и ФПС. Деструктивная свойства# активированных ОК связаны с синтезом широкого спектра протеаз, в первую очередь катепсина К (основной протеолитический фермент ОК). Кроме того, АЦБ, взаимодействуя с виментином, присутствующим на мембране предшественников ОК, обладают способностью индуцировать дифференцировку ОК и тем самым стимулировать резорбцию костной ткани.
О роли гормональных нарушений (связанных с половыми гормонами, пролактином) свидетельствует тот факт, что в возрасте до 50 лет РА наблюдают примерно в 2-3 раза чаще у женщин, чем у мужчин, а в более позднем возрасте эти различия нивелируются. У женщин прием пероральных контрацептивов и беременность снижают риск развития заболевания, а в послеродовом периоде, во время кормления грудью (гиперпролактинемия) риск заболеть существенно повышается.
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
РА является частым и одним из наиболее тяжелых иммуновоспалительных заболеваний человека, что определяет большое медицинское и социально-экономическое значение этой патологии [6]. Распространённость РА среди взрослого населения в разных географических зонах мира колеблется от 0,5 до 2% [2, 7]. По данным официальной статистики, в 2017 году в России зарегистрировано более 300 тысяч пациентов с РА, в то время как по данным Российского эпидемиологического исследования РА страдает около 0,6% от общей популяции [8, 9]. Соотношение женщин к мужчинам — 3:1. Заболевание встречается во всех возрастных группах, но пик заболеваемости приходится на наиболее трудоспособный возраст — 40-55 лет. РА вызывает стойкую потерю трудоспособности у половины пациентов в течение первых 3-5 лет от начала болезни и приводит к существенному сокращению продолжительности их жизни, как за счет высокой частоты коморбидных заболеваний, в первую очередь инфекционных осложнений, так и характерных для РА внесуставных (системные) проявлений (ВП) и осложнений, связанных с системным иммуновоспалительным процессом — ревматоидный васкулит, АА амилоидоз и др. [1, 6].
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
Серопозитивный ревматоидный артрит (М05)
М05.0 Синдром Фелти
М05.1 — Ревматоидная болезнь легкого (J99.0)
М05.2 — Ревматоидный васкулит
М05.3 — Ревматоидный артрит с вовлечением др. органов и систем
М05.8 — Другие серопозитивные ревматоидные артриты
М05.9 — Серопозитивный ревматоидный артрит неуточненный
Другие ревматоидные артриты (М06)
М06.0 — Серонегативный ревматоидный артрит
Источник https://www.diagnos.ru/diseases/ossa/revmartritis
Источник https://www.garant.ru/products/ipo/prime/doc/402775973/