1. Краткая информация по заболеванию или состоянию (группе заболеваний или состояний)
1.1. Определение заболевания или состояния (группы заболеваний или состояний)
Резус-изоиммунизация — наличие в крови матери IgG-антител (анти-Rh (D) антител)
как проявление вторичного иммунного ответа у сенсибилизированных пациенток вследствие несовместимости крови матери и плода по антигенам системы Резус 1 . Синонимы — резус-конфликт, резус-сенсибилизация, резус-аллоиммунизация.
Гемолитическая болезнь плода (ГБП) — заболевание, характеризующееся гемолизом резус(D)-положительных эритроцитов плода под воздействием анти-Rh (D) антител матери, проникающих в кровоток плода через плацентарный барьер, при несовместимости крови матери и плода по системе Резус, и проявляющееся развитием анемии, увеличением числа бластных форм эритроцитов 2 . Синонимы — эритробластоз плода, гемолитическая желтуха.
1.2. Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Резус-изоиммунизация, в основном, развивается при несовместимости крови матери и плода по антигену RhD. Также ГБП может развиться при несовместимости крови матери и плода по антигенам С, с, E, e. Женщина с резус-отрицательной принадлежностью крови сенсибилизируется или во время беременности при попадании в кровоток Rh(D) антигена плода, унаследованного им от биологического отца, или вне беременности при трансфузии компонентов резус(D)-положительной донорской крови.
Во время беременности эритроциты плода проникают через плацентарный барьер в кровоток матери в течение 1-го триместра у 5-7%, во 2-м триместре у 15-16% и в 3-м триместре — у 29-30% женщин 3 . Первым этапом иммунного ответа матери является выработка IgM антител, обладающих высокой молекулярной массой и не проходящих через плацентарный барьер в кровоток плода. Следующими этапами развития изоиммунизации является образование IgG антител, обладающих низкой молекулярной массой и свободно проникающих в кровоток плода от матери через плацентарный барьер, в том числе подклассов иммуноглобулина G1 и G3, которые активно взаимодействуют с Fcрецепторами (FcR) лимфоцитов и макрофагов, играющих важную роль в гемолизе эритроцитов плода.
При 1-й беременности ГБП встречается редко, так как попадание эритроцитов плода в кровоток матери происходит в основном на поздних сроках беременности или во время родов, и первичный иммунный ответ не успевает сформироваться. ГБП при 1-й беременности может быть следствием уже имевшей место изоиммунизации, например, при введении резус-отрицательной женщине компонентов резус-положительной крови в анамнезе.
При последующих беременностях попадание эритроцитов плода в кровоток матери вызывает быстрый иммунный ответ, IgG антитела проникают к плоду, развиваются гемолиз, анемия, активизация очагов экстрамедуллярного кроветворения и гепатоспленомегалия. Вследствие «перегрузки» клеток печени железом и продуктами распада глобина нарушается ее белковая синтетическая функция, что приводит к гипопротеинемии, гипоальбуминемии, а в последующем — к усилению проницаемости стенок сосудов. На фоне прогрессирующей анемии развивается гипоксемия, обуславливающая у плода гипердинамический тип кровообращения, с постепенным формированием сердечной недостаточности и портальной гипертензии, способствующей дальнейшему увеличению размеров печени и возникновению анасарки. Так развивается тяжелая анемия с водянкой плода. При отсутствии проведения внутриутробного лечения может произойти антенатальная гибель плода. Легкая анемия обусловлена более поздним началом гемолиза эритроцитов плода незадолго до родов или сразу после рождения ребенка 3 , 4 .
1.3. Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Гемолитическая болезнь новорожденного (ГБН) (следствие ГБП) в Российской Федерации диагностируется приблизительно у 0,6%-1% новорожденных, при этом частота развития резус-изоиммунизации за последние годы еще не имеет существенной тенденции к снижению 3 . Перинатальная смертность при ГБН составляет 0,037‰. Согласно 32-й форме Росстата в 2014-2016 гг. ГБН в России была диагностирована у 0,9–1,0% новорожденных 3 . Летальность при ГБН в России составляет около 0,22%. Заболеваемость билирубиновой энцефалопатией в различных странах мира находится в диапазоне от 0,4 до 2,7 на 100 000 новорожденных 5 .
1.4. Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
P55 — Гемолитическая болезнь плода и новорожденного.
P55.0 — Резус-изоиммунизация плода и новорожденного.
P55.8 — Другие формы гемолитической болезни плода и новорожденного.
P55.9 — Гемолитическая болезнь плода и новорожденного неуточненная.
P56 — Водянка плода, обусловленная гемолитической болезнью.
P56.0 — Водянка плода, обусловленная изоиммунизацией.
P56.9 — Водянка плода, обусловленная другой неуточненной гемолитической болезнью.
1.5. Классификация заболевания или состояния (группы заболеваний или состояний)
Формы ГРП по характеру иммунологического конфликта между кровью матери и плода:
Формы ГБП по тяжести анемии и наличию водянки плода:
Формы ГБП по уровню гемоглобина/гематокрита у плода:
1.6. Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Основная роль в диагностике ГБП отводится лабораторным и функциональным методам исследования, по которым диагностируется ГБП и устанавливается ее форма.
2. Диагностика заболевания или состояния (группы заболеваний или состояний), медицинские показания и противопоказания к применению методов диагностики
Критерии установления диагноза
Диагноз ГБП устанавливается у резус-отрицательной пациентки, дискордантной с биологическим отцом ребенка по резус-фактору, на основании клинической картины многоводия и отека плода по данным ультразвукового исследования (УЗИ) плода и лабораторных данных в виде анемии и увеличения числа бластных форм эритроцитов у плода.
2.1. Жалобы и анамнез
Специфические жалобы отсутствуют. При развитии тяжелой анемии и водянки плода беременная может отмечать снижение интенсивности шевелений, что является отражением слабой двигательной активности плода на фоне развития у него сердечной недостаточности.
Уровень убедительности рекомендаций С (уровень достоверности доказательств — 5).
1 : Акушерство: национальное руководство / под ред. Г.М. Савельевой, Г.Т. Сухих, В.Н. Серова, В.Е. Радзинского. — 2-е изд. — М.: ГЭОТАР-Медиа, 2018 г.
2 Акушерство: национальное руководство / под ред. Г.М. Савельевой, Г.Т. Сухих, В.Н. Серова, В.Е. Радзинского. — 2-е изд. — М.: ГЭОТАР-Медиа, 2018 г.
Уровень убедительности рекомендаций С (уровень достоверности доказательств — 5).
2.2. Физикальное обследование
Физикальное обследование проводится согласно клиническим рекомендациям
«Нормальная беременность». 3
3 Клинические рекомендации «Нормальная беременность» http://prof.ncagp.ru/index.php?_t8=85
2.3. Лабораторные диагностические исследования
Уровень убедительности рекомендаций В (уровень достоверности доказательств — 1).
Комментарии: Если профилактика резус-изоиммунизации проводится позже 28 недель беременности, то определение анти-Rh-антител проводится перед введением антирезусного иммуноглобулина 8 . Более частое определение анти-Rhантител нецелесообразно. Следует определить резус-фактор мужа/партнера. При резус-отрицательной принадлежности крови мужа/партнера определение антирезусных антител не проводится. При неизвестной или резус-положительной принадлежности крови мужа/партнера беременной женщине желательно провести неинвазивное определение резус-фактора плода по циркулирующим в крови матери внеклеточным фрагментам плодовой ДНК, которое имеет чувствительность и специфичность 98-100%. Это исследование можно рекомендовать в сроке 12 недель беременности во время проведения первого пренатального скрининга. При определении резус-отрицательной принадлежности крови у плода определение антирезусных антител в крови матери не проводится. При отсутствии возможности определения резус-генотипа плода беременность наблюдается как беременность резус-положительным плодом. В европейской популяции преобладает полная делеция гена RhD, что и позволяет выявлять ген RhD плода в кровотоке матери при отсутствии материнского гена. Однако, у 3-5% резус-отрицательных европейцев ген RhD обнаруживается либо полностью, либо как возникший вследствие генной конверсии между экзонами генов RhD и RhCE (гибридные гены RhD-CE-D). Такие гибридные гены не способны кодировать синтез антигена D на поверхности мембраны эритроцитов. В этом случае имеет место расхождение между фенотипической и генотипической резус-принадлежностью. Наличие RhD гена у матери мешает выявлению RhD гена плода. При выявлении RhD гена у матери неинвазивное определение резус-принадлежности плода невозможно, и такая беременность должна быть проведена как беременность резус-положительным плодом.
Комментарий: Снижение гемоглобина на ≥15% от нормы для данного гестационного срока свидетельствуют о развитии тяжелой анемии и является показанием для внутриутробного переливания плоду эритроцитной массы, отмытой от лейкоцитов и тромбоцитов (ЭМОЛТ). Нормативные показатели гемоглобина представлены в таблице 1 (Приложение Б).
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
2.4. Инструментальные диагностические исследования
Уровень убедительности рекомендаций С (уровень достоверности доказательств –5).
Комментарии: Увеличение МССК СМА для соответствующего срока беременности с высокой чувствительностью и специфичностью свидетельствует о развитии у плода гипердинамического типа кровообращения, а повышение значений этого показателя более 1,5 МоМ характерно для тяжелой анемии, требующей вмешательства в течение беременности 4 , 9 , 10 , 11 , 12 . Использование МССК СМА плода позволило значительно снизить необходимость применения кордоцентеза в целях получения крови плода. После 35 недель беременности диагностическая точность данного исследования снижается.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Существует вероятность досрочного экстренного родоразрешения в виду развития осложнений при проведении внутриутробных вмешательств, что может потребовать оказания специализированной и высокотехнологичной неонатальной помощи.

Рисунок 1. Оценка степени выраженности анемии плода в зависимости от максимальной систолической скорости кровотока в средней мозговой артерии плода и срока беременности
А – наличие у плода умеренно тяжелой/тяжелой анемии.
В – отсутствие у плода умеренно тяжелой/тяжелой анемии.
С – отсутствие у плода анемии.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Выявление при УЗИ плода асцита и анасарки (сочетание гидроперикарда, гидроторакса, отека подкожной клетчатки головы, туловища и конечностей плода) является запоздалым свидетельством крайне тяжелого течения ГБП.
2.5. Иные диагностические вмешательства
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
3.1. Медикаментозная терапия
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Эффективных методов медикаментозной терапии резусизоиммунизации и ГБП в настоящее время не существует.
3.2. Внутриутробные переливания ЭМОЛТ плоду
- Рекомендовано для лечения тяжелых форм ГБП применять внутриутробные внутрисосудистые переливания плоду ЭМОЛТ 5 , 13 (Приложение Г).
Уровень убедительности рекомендаций В (уровень достоверности доказательств — 1).
Комментарий: Внутриутробные переливания могут проводиться многократно, последнее переливание обычно проводится в 32 недели беременности и массе плода 2000 г, однако в последние годы имеется тенденция в проведении переливаний в 35-36 недель беременности, что позволяет проводить родоразрешение при сроке 37 недель. Подобный подход уменьшает число осложнений, связанных с недоношенностью новорожденных. Перед проведением внутриутробного переливания крови плоду или при планировании родоразрешения до достижения срока 34 недели однократно проводится профилактика респираторного дистресс-синдрома по стандартной схеме. 6
6 Клинические рекомендации «Преждевременные роды» http://prof.ncagp.ru/index.php?_t8=85
3.3. Родоразрешение при резус-изоиммунизации
7 Акушерство: национальное руководство / под ред. Г.М. Савельевой, Г.Т. Сухих, В.Н. Серова, В.Е. Радзинского. — 2-е изд. — М.: ГЭОТАР-Медиа, 2018 г.
Уровень убедительности рекомендаций С (уровень достоверности доказательств — 5).
Комментарий: При тяжелой анемии плода, отечной форме ГБП, а также после внутриутобного переливания плоду ЭМОЛТ предпочтительно оперативное родоразрешение, так как кесарево сечение позволяет избежать дополнительной травматизации и гипоксии плода во время родов.
4. Медицинская реабилитация, медицинские показания и противопоказания к применению методов реабилитации
Гемолитическая болезнь (ГБН) — симптомы и лечение
Что такое гемолитическая болезнь (ГБН)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Руденко Анастасии Александровны, неонатолога со стажем в 7 лет.
Над статьей доктора Руденко Анастасии Александровны работали литературный редактор Юлия Липовская , научный редактор Наталья Бычкова и шеф-редактор Лада Родчанина

Неонатолог Cтаж — 7 лет
Перинатальный центр №2 на Архиерейской
Областная больница Святителя Иоасафа
Дата публикации 6 ноября 2020 Обновлено 26 апреля 2021
Определение болезни. Причины заболевания
Гемолитическая болезнь новорождённого (ГБН) — это заболевание, при котором эритроциты новорождённого разрушаются антителами матери. Это происходит из-за несовместимости крови матери и ребёнка по антигенам эритроцитов (красных кровяных клеток), чаще всего по резус-фактору и системе групп крови, реже по другим факторам крови.
Чтобы разобраться, что такое гемолитическая болезнь, необходимо понимать значение некоторых терминов:
- Антиген — это любое вещество, которое организм воспринимает как чужеродное и против которого вырабатывает антитела.
- Антитела — это белковые молекулы, с помощью которых организм нейтрализует чужеродные клетки.
- Антигены эритроцитов ( эритроцитарные антигены) — это молекулы, которые находятся на поверхности эритроцитов.
- Гемолиз — разрушение эритроцитов.
Известно более 250 эритроцитарных антигенов, которые образуют более 20 антигенных систем. Однако наиболее важное клиническое значение имеют антигены резус-фактора (Rh) и системы групп крови (АВ0).
Система резус-фактора
Резус-фактор — белок, который может содержаться на поверхности эритроцитов . Кровь считается резус-положительной (Rh+), если на красных кровяных клетках человека есть резус-фактор (антиген D). Если этого антигена на эритроцитах нет, то кровь является резус-отрицательной (Rh-). У большинства людей кровь резус-положительная.
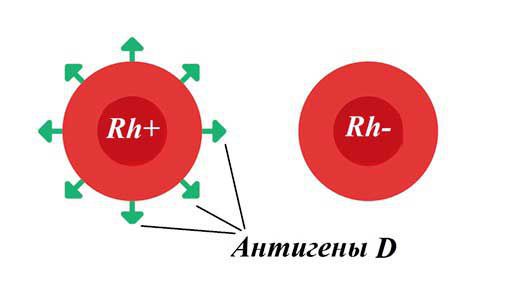
Резус-несовместимость возникает тогда, когда у матери резус-отрицательная кровь, а у ребёнка резус-положительная. В этом случае иммунная система матери может распознавать эритроциты плода как «инородные» и потенциально опасные и вырабатывать антитела против резус-фактора на эритроцитах плода. Антитела прикрепляются к эритроцитам ребёнка и разрушают их (происходит гемолиз). Этот процесс начинается в период его внутриутробного развития и продолжается после рождения. Если плод имеет резус-отрицательную кровь, а мама резус-положительную, конфликта не возникает.
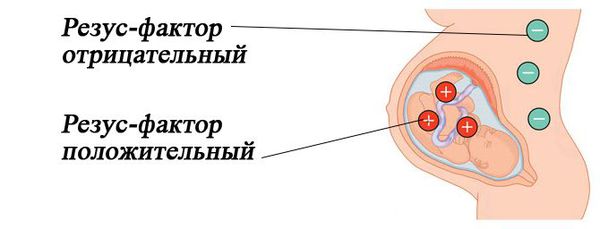
Основными проявлениями ГБН является ранняя желтуха и анемия новорождённого.
В России в 2013 году гемолитическая болезнь новорождённых была диагностирована у 0,83 % детей [1] . Болезнь развивается у одного ребёнка из 20-25 детей, рождённых от женщин с резус-отрицательной кровью [8] .
Система групп крови
Группа крови — это определённое сочетание врождённых антигенов на поверхности эритроцитов и антител в плазме крови. Двумя основными антигенами эритроцитов являются А и В. Группы крови определяются на основании наличия или отсутствия этих антигенов. Одноимённые антитела обозначаются греческими буквами α и β.
Кровь любого человека может одновременно содержать только противоположные антигены и антитела или не иметь каких-то из них. В противном случае должна произойти агглютинация (склеивание) клеток крови. Этот процесс может привести к летальному исходу из-за формирования тромбов и закупорки кровеносных сосудов.
В зависимости от сочетания антигенов и антител различают четыре группы крови по системе АВ0.
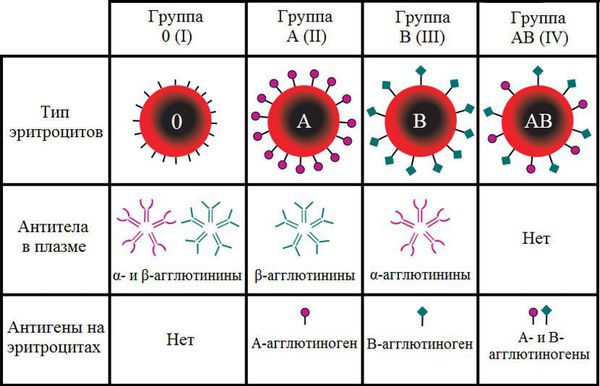
Несовместимость по системе групп крови (АВ0) может возникнуть, если у матери I (О) группа крови, а у плода II (A) или III (B). В этом случае организм матери производит антитела к А или B антигенам, которые могут проникнуть через плаценту, присоединиться к эритроцитам плода и вызвать их разрушение (гемолиз). В результате у плода развивается анемия, однако она менее тяжёлая, чем при резус-несовместимости. В связи с этим несовместимость по системе групп крови не всегда диагностируют и существует предположение, что встречается она намного чаще [3] .
Среди перинатальной смертности гемолитическая болезнь новорождённых занимает 5 место [2] .
Группы риска по развитию данной патологии:
- Дети, имеющие A (II), B (III) или AB (IV) группы крови, рождённые от матерей с 0 (I) группой крови.
- Дети с резус-положительным фактором, рождённые от матерей с резус-отрицательным фактором.
- Дети с редкими антигенами, определяющими группу крови или резус-фактор, рождённые от матерей, у которых отсутствуют данные антигены.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы гемолитической болезни
Во время беременности признаки несовместимости крови матери и плода не проявляются.
Клиническая картина гемолитической болезни новорождённых зависит от проявления одной из трёх форм: анемической, желтушной и отёчной. Но может иметь место сочетание клинических форм.
1. Анемическая форма ГБН. Является наиболее лёгкой формой и проявляется бледностью кожных покровов, неврологическими нарушениями (вялость: ребёнок неохотно сосёт грудь, много спит) и признаками увеличения печени и селезёнки, которые наблюдаются в динамике.
2. Желтушная форма ГБН. Встречается чаще всего — до 90 % случаев [8] . Основной симптом в этом случае — желтуха. Кожа и видимые слизистые оболочки становятся жёлтыми в первые часы после рождения (до 24 часов), также могут быть увеличены печень и селезёнка (гепатоспленомегалия). Степень тяжести желтушной формы будет зависеть от интенсивности (яркости) и распространённости желтухи на теле новорождённого, что доктор может определить визуально с помощью шкалы Крамера.
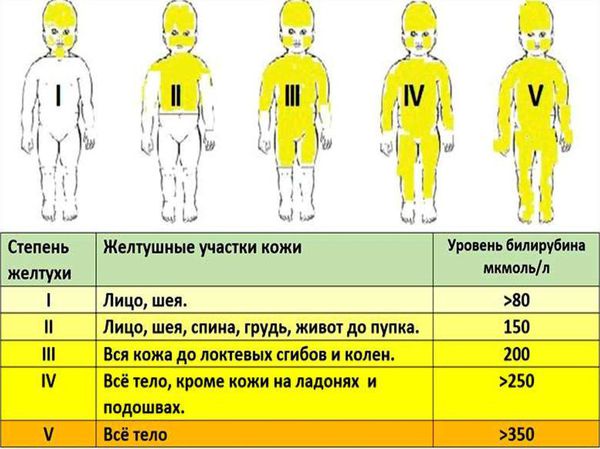
Интенсивность желтухи будет зависеть от уровня билирубина ( жёлчного пигмента, который образуется при разрушении эритроцитов ). Именно билирубин окрашивает кожу в жёлтый цвет. При достижении критических цифр этот фермент может поражать нейроны головного мозга, что приводит к повреждению его структур и развитию грозного осложнения — билирубиновой энцефалопатии (ядерной желтухи).
3. Отёчная форма ГБН («водянка плода»). Является наиболее тяжёлой формой заболевания. В большинстве случаев она диагностируется ещё внутриутробно. При рождении обращают на себя внимание желтушно окрашенные плодные оболочки, околоплодные воды, первородная смазка и пуповина. С первых минут жизни ребёнок находится в тяжёлом состоянии, для которого характерны выраженные отёки, распространённые по всему телу: подкожный отёк (анасарка), в области живота и органов брюшной полости (асцит), в области грудной клетки (гидроперикард) [4] .
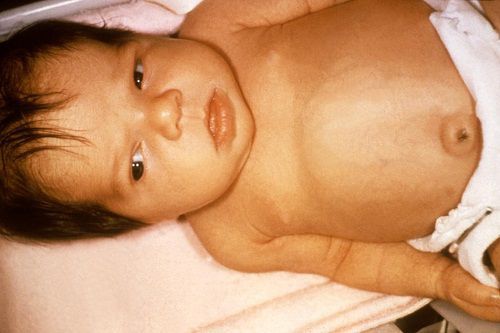
Кожа и видимые слизистые новорождённого бледно-розовые, могут иметь слегка желтоватый оттенок, печень и селезёнка увеличены — всё это обусловлено повышенным распадом эритроцитов, что приводит к анемии. Дети с такой формой заболевания нуждаются в интенсивном лечении, включающем в себя операцию заменного переливания крови (ОЗПК).
Патогенез гемолитической болезни
Развитие гемолитической болезни возможно лишь при контакте крови матери и плода. Во время беременности благодаря плаценте эритроциты плода попадают в организм матери в незначительном количестве, недостаточном для выработки антител. В момент родоразрешения, вследствие абортов, выкидышей или осложнённых беременностей эритроциты проникают в кровоток матери в большом количестве, что вызывает выработку антител класса М (IgM). Эти антитела образуются почти сразу после контакта с резус-положительной кровью плода. Они обеспечивают временный иммунитет от любых чужеродных веществ, однако IgM не способны проникать через плаценту к ребёнку.
Антитела класса М затем трансформируются в антитела класса G (IgG). Они вырабатываются через 3 месяца после контакта с резус-положительными эритроцитами, обеспечивают длительный иммунитет в течение нескольких лет и способны пройти через плаценту в кровь плода. Этим объясняется тот факт, что при первой беременности эти иммунные частицы для плода не опасны, ведь при нормально протекающей беременности кровь ребёнка смешивается с кровью матери лишь на последних месяцах беременности или после родов, когда IgG ещё не выработались.
При первой беременности происходит лишь узнавание эритроцитов плода, т. е. первичный иммунный ответ, который ещё называют «раздражением» иммунной системы матери. Также для этого процесса используется термин «сенсибилизация», а применимо к резус-конфликту — «резус-сенсибилизация». Первичный иммунный ответ не опасен для плода.
Как правило, конфликт по резус-фактору развивается при повторной беременности. Это связано с тем, что к моменту следующего зачатия в организме матери уже присутствуют антитела класса G, поэтому они начинают атаковать эритроциты плода уже на ранних сроках. В связи с этим вероятность развития данного заболевания, как и тяжесть, растёт с каждой последующей беременностью. Болезнь встречается у 63 % детей от женщин с сенсибилизацией.
Важно понимать, что в случае аборта при первой беременности, независимо от способа его проведения, вероятность возникновения сенсибилизации (выработки антител) у женщин с отрицательным резус-фактором значительно увеличивается. Вместе с тем увеличивается и риск бесплодия .
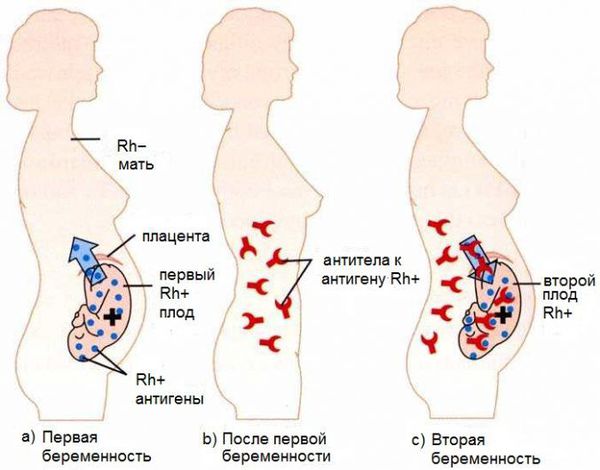
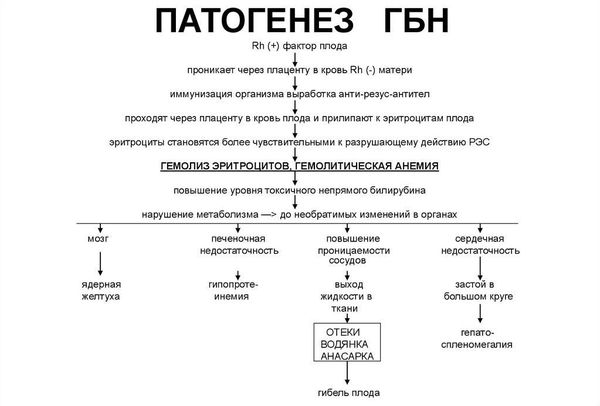
Материнские антитела разрушают эритроциты плода в печени и селезёнке, что нарушает работу этих органов. При большом количестве антител поражение красных клеток крови происходит внутри сосудов. В ответ на гибель эритроцитов печень, селезёнка и костный мозг начинают вырабатывать ретикулоциты (клетки-предшественники эритроцитов), что приводит к их увеличению. Это объясняет развитие симптома анемии и гепатоспленомегалии (увеличения печени и селезёнки) [7] .
Продуктом распада эритроцитов является непрямой билирубин — желчный пигмент. Билирубин является токсичным ферментом, который повреждает ткани головного мозга, печени, лёгких, почек и т. д. Критическое повышение уровня непрямого билирубина приводит к необратимому повреждению структур головного мозга — билирубиновой энцефалопатии (ядерной желтухе).
Факторами развития ядерной желтухи являются недоношенность, инфекции, гипоксия ( недостаток кислорода у плода) , метаболические нарушения (сниженный или повышенный уровень глюкозы в крови), кровоизлияния, приём некоторых лекарственных препаратов (сульфаниламиды, салицилаты, фуросемид, диазепам и т. д.) и употребление алкоголя [2] .
Классификация и стадии развития гемолитической болезни
Существует несколько классификаций гемолитической болезни новорождённых [1] . Первая связана с причиной ГБН и зависит от вида иммунологической несовместимости эритроцитов матери и плода:
- несовместимость по резус-фактору;
- несовместимость по системе АВ0 (групповая несовместимость);
- несовместимость по редким факторам крови (RhC, Rhc, RhE, Rhe).
Классификация по ведущим клиническим проявлениям:
- отёчная форма (наиболее тяжёлая);
- желтушная форма (в зависимости от выраженности желтушного синдрома степень ГБН может быть лёгкой, средней и тяжёлой);
- анемическая форма (чаще всего является проявлением лёгкой степени тяжести).
По наличию или отсутствию осложнений:
- неосложнённая форма;
- осложнённая форма (билирубиновая энцефалопатия, синдром сгущения желчи, геморрагический синдром, обменные нарушения).
По степени тяжести:
- Лёгкая степень. Включает в себя незначительные клинические проявления или их отсутствие, лабораторные признаки ГБН. При наличии желтушного синдрома дети нуждаются в фототерапии.
- Средняя степень. Включает в себя клинические и лабораторные проявления ГБН. Дети нуждаются в непрерывной фототерапии, в некоторых случаях — в операции заменного переливания крови.
- Тяжёлая степень. Наличие выраженных клинических проявлений с нарушением работы органов и систем. Выраженные лабораторные изменения, при которых дети нуждаются в интенсивном лечении и операции заменного переливания крови.
Осложнения гемолитической болезни
Самым грозным осложнением гемолитической болезни новорождённых считается билирубиновая энцефалопатия (ядерная желтуха) [7] . Она возникает из-за отравляющего влияния непрямого билирубина на серое вещество головного мозга (базальные ядра). Данные структуры мозга отвечают за двигательную активность, координацию движений и мотивацию в человеческом поведении. Существует 4 фазы ядерной желтухи:
- Первая фаза — билирубиновая интоксикация. Проявляется в первые дни жизни. Женщина может обратить внимание, что ребёнок стал вялым: плохо сосёт грудь, отказывается от еды, срыгивает, плачет не так эмоционально, как раньше. Можно заметить сниженный мышечный тонус, возможны приступы апноэ (остановки дыхания на короткий промежуток времени).
- Вторая фаза — спастическая. Появляется на 3-4 сутки заболевания. Ребёнок занимает вынужденное положение — поза «легавой собаки». Голова ребёнка запрокинута за счёт ригидности (скованности) затылочных мышц, имеется выраженное напряжение мышц конечностей, кисти крепко сжаты в кулак, могут появиться судороги, пронзительный «мозговой» крик (отсутствуют эмоции, крик громкий, резкий), ребёнок не берёт грудь. Поражение головного мозга на данной стадии носит необратимый характер.
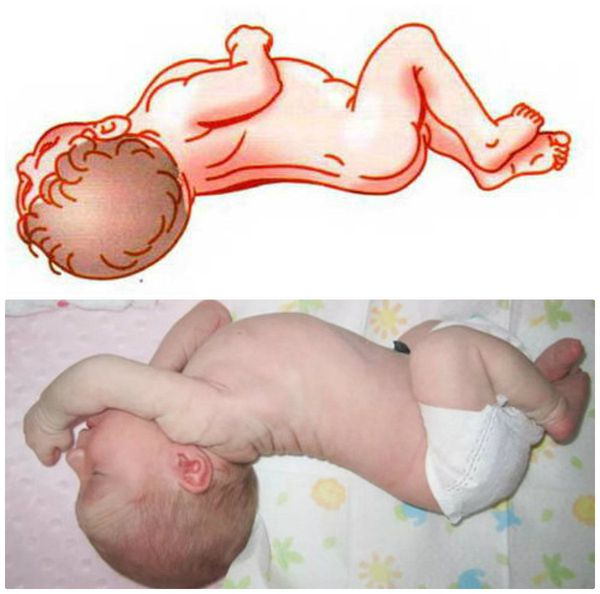
- Третья фаза — мнимого благополучия. Появляется на 2-3 месяце заболевания. Длится несколько недель. Клинические проявления становятся менее выраженными, желтуха уменьшается. У родителей складывается впечатление, что ребёнок выздоравливает.
- Четвёртая фаза — период формирования клинических проявлений. Появляется на 3-5 месяце жизни/заболевания. Появляются грубые неврологические нарушения: параличи, парезы (снижение силы мышц), снижение слуха, отставание в развитии и т. д.
Диагностика гемолитической болезни
Диагноз ГБН может быть заподозрен ещё внутриутробно: на основании анамнеза, данных УЗИ и лабораторных данных.
Женщины, имеющие резус-отрицательный фактор во время беременности должны сдавать анализ крови на определение титров антител (титр анти-D антител) в динамике: при постановке на учёт в женскую консультацию и в течение беременности не менее трёх раз [4] . Рост данного титра может говорить о том, что у плода уже развивается гемолитическая болезнь.
Неинвазивным методом диагностики гемолитической болезни является УЗИ плода. При данном исследовании уже внутриутробно можно заподозрить отёчную форму ГБН.
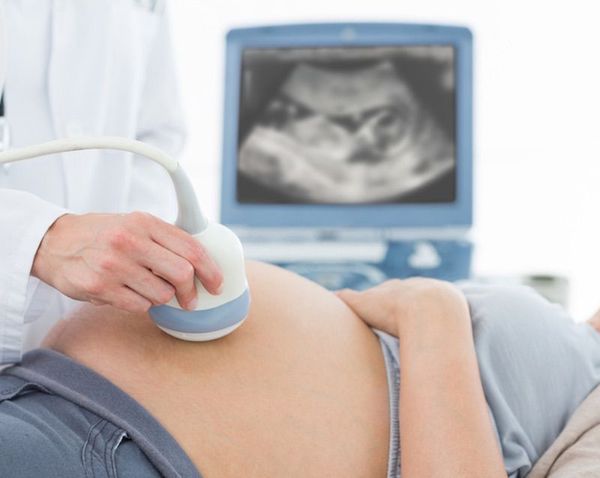
При оценке кровотока средней мозговой артерии во время проведения допплерометрии также можно заподозрить данное заболевание: при анемии скорость кровотока в средней мозговой артерии будет выше нормы [1] .
Сразу после рождения детям из группы риска по развитию гемолитической болезни показано определение группы крови и концентрации общего билирубина в пуповинной крови. Дети, не совпавшие по группе крови или резус-принадлежности с матерью, в течение первых суток жизни несколько раз осматриваются медицинским персоналом [8] . У детей с ГБН уровень билирубина в последующие 72 часа после рождения интенсивно нарастает, почасовой прирост составляет от 0,85 до 3,4 мкмоль/л.
В палате совместного пребывания мама может сама обратить внимание на желтушность кожных покровов, видимых слизистых и склер в первые сутки, а иногда и часы жизни, желтуха будет прогрессировать. Также можно заметить бледность кожи и слизистых.
При подозрении на ГБН неонатолог проводит целый ряд лабораторных исследований, чтобы подтвердить заболевание и определить его форму:
- Общий анализ крови. Можно увидеть анемию (снижение количества эритроцитов), ретикулоцитоз (увеличение количества клеток-предшественников эритроцитов), изменение формы эритроцитов.
- Биохимический анализ крови. Отмечают прогрессирующее повышение уровня непрямого билирубина, снижение уровня альбуминов и т. д.
- Серологические тесты (пробы Кумбса). Прямая проба Кумбса (прямой антиглобулиновый тест) — определение антител, прикреплённых к поверхности эритроцитов. Ярко выраженная положительная проба Кумбса говорит о наличии ГБН по резус-фактору. При групповой несовместимости проба Кумбса слабо положительная в первые сутки и отрицательная со 2-3 суток. Непрямая проба Кумбса — определение антител к эритроцитам в сыворотке крови. Она является более чувствительной и применяется в индивидуальных случаях, когда причину разрушения эритроцитов сложно определить [9] .
Гемолитическую болезнь новорождённых необходимо отличать от других заболеваний:
- наследственных гемолитических анемий;
- постгеморрагических анемий;
- неиммунной водянки плода;
- TORCH-инфекций: токсоплазмоза, цитомегаловирусной инфекции, парвовируса В19, сифилиса;
- обменных нарушений: галазтоземии ( избытка галактозы и её метаболитов ), гипотиреоза ( недостатка гормонов щитовидной железы ), тирозинемии ( отсутствия фермента, необходимого для обмена аминокислоты тирозина ).
Лечение гемолитической болезни
В лечении гемолитической болезни новорождённых используют два подхода: консервативный (фототерапия и инфузионая терапия с применением внутривенных иммуноглобулинов) и оперативный (операция заменного переливания крови) [3] .
Основные критерии выбора тактики лечения: форма гемолитической болезни новорождённых, тяжесть анемии, уровень билирубина и его почасовой прирост.
При отёчной форме ГБН тактика врача будет зависеть от тяжести состояния ребёнка. Как правило ребёнок с такой формой заболевания нуждается в стабилизации общего состояния (проведении искусственной вентиляции лёгких, коррекции метаболических нарушений и т. д.) с дальнейшим проведением операции заменного переливания крови [1] .
Самым эффективным и наиболее безопасным методом лечения ГБН является фототерапия [2] . Этот метод основан на лечебном воздействии ультрафиолетовых лучей с длиной волны 450-500 нм . Уф-лучи проникают через кожу ребёнка и способствуют образованию нетоксичной водорастворимой формы билирубина, которая затем выводится из организма с физиологическими отправлениями . Это снижает уровень билирубина в крови ребёнка и защищает организм от его токсического воздействия
С первых часов постановки диагноза фототерапия должна проводиться в непрерывном режиме. При этом источник света должен находиться от ребёнка на расстоянии не более 50 см. Во время процедуры кожа новорождённого должна быть максимально открытой: предпочтительно оставлять ребёнка в одном подгузнике, а глаза закрывать светонепроницаемыми очками.
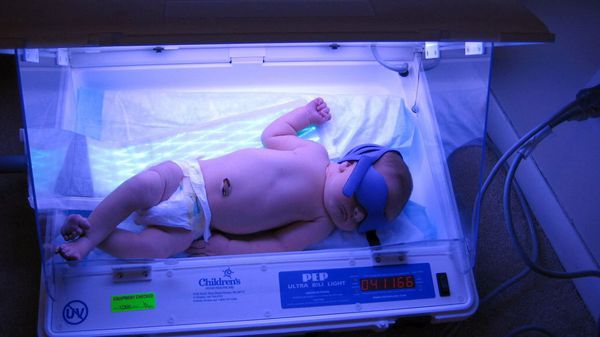
При интенсивной фототерапии потери жидкости из организма новорождённого увеличиваются на 20 %. Восполнить жидкость можно с помощью инфузионной терапии (внутривенного введения) или более частого прикладывания к груди (при недостаточной выработке молока необходимо допаивать ребёнка) [1] .
Побочные эффекты данного вида лечения:
- транзиторная мелкоточечная сыпь на теле (не требует лечения);
- синдром «бронзового ребёнка» (окрашивание мочи, кала и кожи в бронзовый цвет), который регрессирует через несколько недель [5] .
Введение высоких доз внутривенных иммуноглобулинов может уменьшить разрушение эритроцитов, что снижает число операций заменного переливания крови (ОЗПК). Введение данного препарата возможно в течение первых трёх суток жизни с интервалом в 12 часов [1] .
Операция заменного переливания крови проводится при тяжёлых формах гемолитической болезни новорождённых. Она направлена на предотвращение развития билирубиновой энцефалопатии путём выведения из организма ребёнка непрямого билирубина [1] . ОЗПК выполняется в отделении детской реанимации или в палате интенсивной терапии с соблюдением всех правил асептики и антисептики.
Обменное переливание крови проводится через стерильный катетер, введённый в вену пуповины. Суть операции заключается в медленном дробном выведении крови из организма новорождённого с последующим попеременным замещением эритроцитарной массой и плазмой донора в равном количестве.
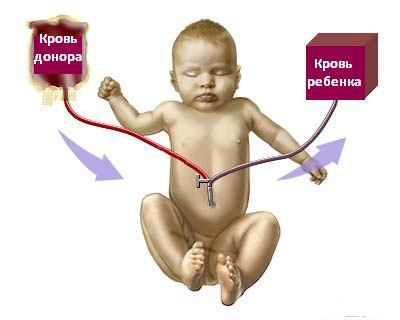
При проведении ОЗПК возможно развитие осложнений: гематологических, инфекционных, метаболических, системных и осложнений со стороны сердечно-сосудистой системы.
Прогноз. Профилактика
Профилактика данного заболевания может быть специфической и неспецифической.
Неспецифическая профилактика: планирование семьи, индивидуальный подбор компонентов крови при трансфузиях (переливаниях компонентов крови), предшествующих беременности, УЗ-скрининг во время беременности, а также предотвращение абортов [8] .
Специфическая профилактика заключается во введении иммуноглобулинов человека антирезус Rh0(D) женщинам с резус-положительным ребёнком. Данная процедура выполняется беременным на сроке 28-30 недель и в первые 72 часа после родоразрешения [5] . Иммуноглобулин быстро покрывает резус-положительные эритроциты плода, которые попали в кровоток матери, после этого они уже не распознаются иммунной системой матери как чужеродные и не вызывают образование антител. Такое лечение, как правило, предотвращает развитие гемолитической болезни новорождённых.
Прогноз. Более 90 % детей, получивших своевременное лечение, впоследствии не имеют неврологических нарушений.
Список литературы
- Диагностика и лечение гемолитической болезни новорождённых. Клинические рекомендации. — М.: ГОЭТАР-Медиа, 2015.
- Володин Н. Н., Дегтярев Д. Н., Крючко Д. С. Неонатология. клинические рекомендации. — М.: ГОЭТАР-Медиа, 2019.
- Иванова А. В., Захарова С. Ю., Пестряева Л. А. Особенности морфологии эритроцитов у детей с гемолитической болезнью новорожденных, перенесших внутриутробное, внутрисосудистое переливание крови // Российский вестник перинатологии и педиатрии. — 2016.
- Исаханов М. А., Шарипова М. Г., Манабаева Г. К., Профилактика и неинвазивная диагностика гемолитической болезни плода // электронный научный журнал UNIVERSUM: медицина и фармакология. — 2019.
- Шабалов Н. П. Неонатология. 2 том. — М.: МЕДпресс-Информ, 2009.
- Володин Н.Н. Неонатология: национальное руководство. — М.: ГОЭТАР-Медиа, 2013.
- Рооз Р., Генцель-Боровичени О., Прокитте Г. Неонатология: практическое руководство. — М.: Медицинская литература, 2010.
- Гемолитическая болезнь новорождённых: лекция / Белорусский государственный университет. — 2019.
- Секреты неонатологии и перинатологии / Р. А. Полин, пер. с англ. под ред. Н. Н. Володина. — М.: Бином, 2011.
- Гемолитическая болезнь плода и новорождённого: клинический протокол МЗ РК. — 2019.
Источник https://spnavigator.ru/document/02637b2c-5525-47b7-b8c6-e2046445186e
Источник https://probolezny.ru/gemoliticheskaya-bolezn/